Les principales voies du métabolisme

Généralités
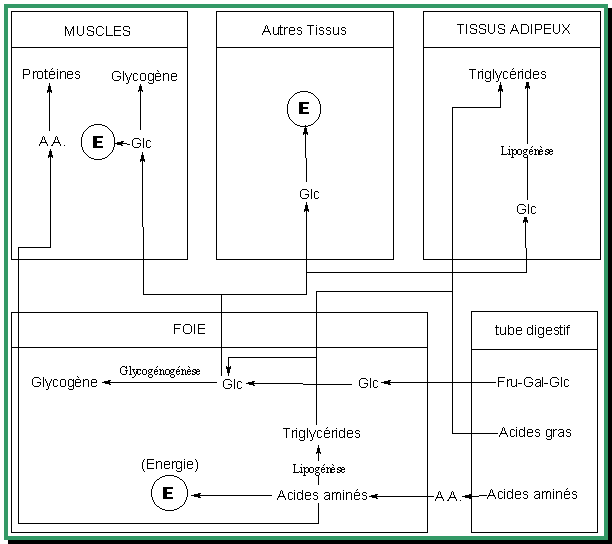
[modifier | modifier le wikicode]Devenir et utilisation des nutriments dans l'organisme
[modifier | modifier le wikicode]Devenir des nutriments après le repas
[modifier | modifier le wikicode]- Les triglycérides :
- Lieu de stockage : tissus adipeux selon 3 origines (acides gras, acides aminés et glucose)
- Une fraction est oxydée dans tous les organes
- Les acides aminés (A.A.) :
- Source d'énergie pour le foie
- Peuvent être transformés en acides gras et certains en glucose
- Participation aux synthèses protéiques dans toutes les cellules
- Le glucose :
- Source d'énergie principale
- Stockage dans le foie et les muscles
- Transformation en triglycérides et stockage dans le tissus adipeux
Devenir des nutriments lors d'une période de jeûne (de courte durée)
[modifier | modifier le wikicode]Problème essentiel : maintenir la glycémie constante car le système nerveux ne peut utiliser que le glucose comme source d'énergie. Or le glucose n'est plus absorbé au niveau du tube digestif (période de jeûne). Les sources de glucose sanguin sont au nombre de 4 : Glucose hépatique et les 3 voies de la néoglucogenèse. Les Triglycérides sont la première source d"énergie utilisée en cas de jeûne. Si la période de jeûne est de courte durée, les réserves de glycogène suffisent.
Si la période de jeûne est de longue durée, il se produira une protéolyse afin de transformer les acides aminés en glucose et tous les organes (sauf le cerveau) utiliseront les acides gras comme source d'énergie afin d'épargner au maximum la glycémie.
Notions d'énergétique
[modifier | modifier le wikicode]Qu'est-ce que l'énergie ?
[modifier | modifier le wikicode]C'est la capacité à effectuer un travail. Toutefois, cette énergie existe sous deux formes : énergie cinétique (énergie de mouvement, eg : la pierre qui tombe) ou énergie potentielle (énergie de position, eg : énergie contenue dans la pierre).
Les deux énergies sont inter-convertibles soit de façon spontanée (c'est la pierre qui tombe et qui passe de son niveau énergétique haut à son niveau énergétique bas = réaction exergonique), soit de façon non spontanée (c'est la pierre qui remonte vers son niveau énergétique haut : il faut pour se faire apporter de l'énergie à la pierre = réaction endergonique).
Toutefois, pour libérer l'énergie potentielle et transformer celle-ci en énergie cinétique il faut une énergie d'activation (eg : la clé que l'on tourne dans la voiture démarre le moteur)
Unités énergétique : kJ (le kilojoule) Couplage énergétique : Les réactions endergoniques sont couplées à des réactions exergoniques.
Application avec le Glucose :
[modifier | modifier le wikicode] à corriger : fin de la réaction 38H2O + 38 ATP (il manque le 38 devant ATP)
à corriger : fin de la réaction 38H2O + 38 ATP (il manque le 38 devant ATP)
Rendement de la réaction : (R=41,2%)
La molécule énergétique :
[modifier | modifier le wikicode]- A = Adénosine (Adénine + Ribose)
- T = Tri
- P = Phosphate
- A = Adénosine
- D = Di
- P = Phosphates
attention à la lecture de ce graphique : il n'y a que 2 liaisons à haut potentiel et non pas 4
- Adénosine + Acide phosphorique (Pi) + 10,5 kJ ⇒ adénosine mono-phosphate + H2O
- AMP + Pi + 30,5 kJ ⇒ ADP + H2O
- ADP + Pi + 30,5 kJ ⇒ ATP + H2O
L'ATP (au niveau cellulaire) ne sert pas vraiment à stocker de l'énergie (dans la cellule on stocke l'énergie sous forme de glycogène) ; par contre c'est une molécule de transfert énergétique : elle peut transporter l'énergie là où l'on en a besoin.
On a besoin de sous pour vivre. Le lieu de stockage est la banque (foie) qui stocke sous forme de lingots d'or (glycogène). Nous, on ne paye pas en lingots mais en petites pièces (ATP). Nous dépensons en fonction de nos besoins. Nous avons besoin de ressources pour fournir l'argent à la banque (petit-déjeuner, déjeuner…).
Les coenzymes
[modifier | modifier le wikicode]Le métabolisme énergétique (eg : réaction d'oxydation cellulaire du glucose : C6H12O6 + 6 O2 ⇒ 6 CO2 + 6 H2O) ne s'effectue pas en une seule étape mais nécessite l'intervention de nombreuses réactions enzymatiques. Les principales étant des réactions de déshydrogénation et de décarboxylation. Les deux réactions se font par le biais d'enzymes décarboxylases et déshydrogénases. Ces enzymes ne peuvent travailler seules. Il leur faut l'aide de coenzymes.
Qu'est-ce qu'un coenzyme ? C'est une molécule qui aide l'enzyme à fonctionner.
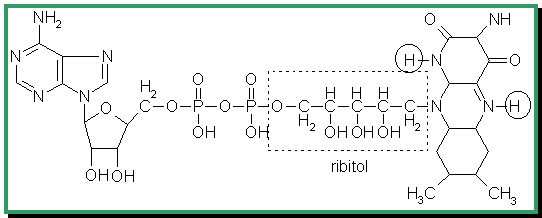
NAD = Nicotinamide Adénine Dinucléotide
- Nicotinamide : synthétisé par vitamine PP ou tryptophane = acide aminé essentiel
- Adénine : base azotée
- Dinucléotide : 2 riboses
sur le schéma : NAD (les deux en haut) et NADP (la réaction du bas)
Rappel :
[modifier | modifier le wikicode]Équation enzymatique : E+S⇒ES⇒E+P
Classes enzymatiques : oxydoréductases, transférases, hydrolases, lyases, isomérases, ligases
Certains enzymes ne travaillent qu'en présence d'une coenzyme.
Une coenzyme est une molécule organique spécifique thermostable et de faible poids moléculaire. L'ensemble enzyme & coenzyme constitue l'holoenzyme (apoenzyme + coenzyme). La coenzyme peut être liée de façon covalente ou non à l'apoenzyme. Si la coenzyme est liée de façon covalente on parlera de groupe prosthétique (eg : hémoglobine ⇒ le fer est le cofacteur, le coenzyme).
Les enzymes nécessitant des coenzymes sont :
- Oxydoréductases
- Transférases
- Isomérases
- Ligases
Les enzymes ne nécessitant pas de coenzymes sont :
- Hydrolases
- Lyases
La coenzyme est souvent envisagée comme cosubstrat de la réaction ou second substrat réactionnel :
Rôle des coenzymes comme réactifs de transfert de groupe
[modifier | modifier le wikicode]Eg : déshydrogénation ou transamination.
Équation globale : D-G+A ⇒ A-G+D
| élément | enzymes |
|---|---|
| Fe2+ / Fe3+ | Cytochromes, peroxydases, catalases |
| Cu+ / Cu2+ | Cytochrome oxydase, tyrosinase |
| Mg2+ | Phosphotransférase |
| Mn2+ | Arginase, enzyme à biotine |
| Zn2+ | Alcool déshydrogénase, anhydrase carbonique |
| K+ | Pyruvate kinase |
| Na+ | Pompe sodium – potassium |
| Mo3+ / Mo6+ | Xanthine oxydase, sulfite oxydase |
| Se | Glutathion peroxydase |
| Cl- | α-amylase, enzyme de conversion |
| Ni2+ | Uréase |
| Ca2+ | Phosphorylase kinase |
| Coenzyme et abréviation | Vitamine ou facteur de croissance apparente | Principales fonctions | |
|---|---|---|---|
COENZYMES DES OXYDOREDUCTASES
| |||
| I- | Nicotinamide-adénine-dinucléotide (NAD) Nicotinamide-adénine-dinucléotide-phosphate (NADP) |
Tryptophane, nicotinamide | Oxydoréduction (déshydrogénase, oxygénases, transporteurs de la chaîne respiratoire) |
| II- | Flavine-mononuclétide (FMN) Flavine-adénine-dinucléotide (FAD) |
Vitamine B2 ou riboflavine | |
| III- | Groupement prosthétiques des cytochromes | ||
| IV- | Coenzymes quinoniques (ubiquinones) | ||
| V- | Tétrahydrobioptérine | Aucun | Hydroxylation Phe, Tyr, Trp |
COENZYMES DES AUTRES CLASSES
| |||
| I- | Carboxylations, décarboxylations
|
|
|
| II- | Transferts de radicaux monocarbonés (sauf carboxyle)
|
|
|
| III- | Transfert d'acyle Coenzyme A (CoA-SH) |
Acide pantothénique | |
| IV- | Nucléotides et dérivés
|
| |
| V- | Métabolisme des amino-acides Phosphate de pyridoxal (PAL) |
Vitamine B6 ou pyridoxine | |
| VI- | Isomérisations Adénosylcobalamine |
Vitamine B12 (cobalamine) | |
Le métabolisme des glucides
[modifier | modifier le wikicode]
La glycogénogenèse
[modifier | modifier le wikicode]- 1 glucokinase (= kinase : ajoute un acide phosphorique)
- 2 phosphoglucomutase = mutase
- 3 UDP glucophosphorylase
- 5 Glycogénosynthase
- 6 enzyme branchante
Glycogénolyse
[modifier | modifier le wikicode]Seul le Glc est capable de passer la membrane cytoplasmique, G1P ou G6P sont incapables de sortir de la cellule.
- Phosphorylase
- Phosphoglucomutase
- Glucose phosphatase
La glucose phosphatase n'existe que dans le foie. Dans le muscle il y a aussi une réserve de glycogène.
La glycolyse
[modifier | modifier le wikicode]S'effectue dans toutes les cellules sauf les adipocytes (utilisent les acides gras) et le foie (utilise les acides aminés).
Cet ensemble de réactions s'effectue dans le cytosol.
Glycolyse s'effectuant en milieu ANAEROBIE ( absence d'oxygène) .
Devenir des 2 molécules de pyruvate
[modifier | modifier le wikicode]Deux devenir différents suivant la situation anaérobie (O2) ou aérobie (O2).

définition:la glycolyse est la séquence de réactions enzymatiques conduisant à la transformation, dans le cytosol,du glucose en pyruvate stratégie chimique : phosphorylation du glycose et conversion d'intermédiaires phosphorylés en composés à haut potentiel de transfert de groupements phosphate et transfert de groupements phosphate conduisant à la synthèse d'ATP.
La chaîne respiratoire
[modifier | modifier le wikicode](régénération des coenzymes réduits)
Les coenzymes sont dans la matrice mitochondriale. La chaîne respiratoire va permettre de régénérer les coenzymes réduits.
Ces réactions d'oxydoréduction s'effectuent au niveau de la membrane interne de la mitochondrie et à l'aide d'enzymes et de coenzymes à savoir des enzymes de transport de protons (H+) du transporteur réduit (NAD ou FAD) du O2 et d'autre part des enzymes de couplage énergétique le tout constitue la chaîne respiratoire.
But de la chaîne respiratoire : faire passer des protons et des électrons d'un potentiel le plus électronégatif vers un potentiel le plus électropositif.
Les protons libérés dans l'espace inter membranaire par le CoEQ ressortent vers la matrice de la mitochondrie via un complexe F0/F1.
F0 = canal protéique à protons
F1 = complexe ATP/synthétase
Le transfert des 2 protons au travers de F0 permet de faire fonctionner F1 et donc de fabriquer une molécule d'ATP dans l'espace inter-membranaire, H+ rencontre O2 qui le capte pour former de l'eau.
Cycle de Krebs
[modifier | modifier le wikicode]Dans la matrice de la mitochondrie
Métabolisme des acides aminés
[modifier | modifier le wikicode]Devenir des protéines alimentaires
[modifier | modifier le wikicode]Alimentation ⇒ protéines alimentaires (végétales et animales) ⇒ acides aminés (par l'action de protéases)
Acides aminés non-indispensables, indispensables (Tryptophane, Lysine, Leucine, Isoleucine, Valine, Thréonine, Méthionine, Phénylalanine), acides aminés pseudo indispensables (Arginine, Histidine).
Le "turn-over" des protéines tissulaires est de 1 à 2% (par jour ? information lacunaire à ce niveau). C'est à dire que 1 à 2% des protéines tissulaires sont dégradés en acides aminés. 75% des acides aminés obtenus servent à synthétiser d'autres protéines. Le reste est soit dégradé sous forme de déchets (urée), soit on en fait des glucides ou des corps cétoniques. Ce qui signifie que la perte nette journalière en protéines est de 30/40g. Pertes en azote de 5 à 7g/jour.
Il n'y a pas de stockage d'acides aminés.
Bilan de N : équilibre : entrées = sorties
Mais parfois ce bilan peut être positif Entrée > Sortie
(eg : femme enceinte, nourrisson, adolescent)
Ou bien peut être négatif Entrée < Sortie
(eg : personnes atteintes de maladies nutritionnelles ; anorexie, Kwashiorkor)
Catabolisme des acides aminés
[modifier | modifier le wikicode]Désamination oxydative
[modifier | modifier le wikicode]Réaction de transamination
[modifier | modifier le wikicode]réaction de transfert de la fonction amine
 Attention à gauche: le deuxième acide est un acide cétonique
Attention à gauche: le deuxième acide est un acide cétonique
Réaction de décarboxylation
[modifier | modifier le wikicode]Couplage désamination-transamination
[modifier | modifier le wikicode]Devenir de l'ammoniac
[modifier | modifier le wikicode]Cycle de l'urée : consomme 4 molécules d'ATP par molécule d'urée synthétisée
Cette voie est consommatrice d'ATP : l'organisme doit dépenser de l'énergie pour ce processus de détoxication.
Bilan énergétique : - 4 ATP / molécule d'urée synthétisée.
Le métabolisme des lipides
[modifier | modifier le wikicode]Acides Gras : entrent dans un cycle de β-oxydation au niveau de la matrice mitochondriale β-oxydation des acides gras (matrice mitochondriale), les réactions se font en chaîne et on l'appelle "hélice de Lynen".
Bilan : pour un acide gras en C18 (18/2=9 ; 9-1=8; 8 tours d'hélice)
pour un C24 : 12-1= 197 ATP
eg : lorsque l'on mange une religieuse au chocolat et que l'on ne dépense pas ce sucre par un footing, le glucose ne se dirige pas vers le Cycle de Krebs mais vers les Acides Gras. Il y a conservation d'un peu de sucre pour fabriquer du glycérol (glycérol + 3 acides gras = triglycéride).
La transformation du glucose en acides gras + glycérol = triglycéride s'appelle la lipogenèse (a lieu dans le foie et les tissus adipeux).