Le noyau atomique/Introduction historique : la découverte du noyau atomique

Dans ce chapitre, nous allons voir comment la science a progressivement découvert la structure de l'atome et a découvert le noyau atomique. Le sujet en question déborde un petit peu de la simple étude du noyau atomique (nous verrons un petit peu de chimie dans ce chapitre), mais cela donnera une bonne base pour la suite du cours. Nous allons commencer notre périple au début des années 1900. À cette époque, la physique savait que la matière était composée d'atomes, mais elle ne savait pas ce qu'il y avait dedans.
L'état de la physique atomique au début du 19ème siècle
[modifier | modifier le wikicode]Dès le 19ᵉ siècle, certains scientifiques avaient l'intuition que l'atome était composé de particules plus simples, sans toutefois réussir à le prouver. L'un d'entre eux était le médecin anglais William Prout, qui émit cette hypothèse dans un article paru en 1815. Prout étudiait la masse des atomes et il fit une remarque intéressante : la masse d'un atome est proportionnelle à la masse du noyau d'hydrogène. Une conclusion naturelle de cette observation était que l'atome était composé de plusieurs atomes d'hydrogènes reliés entre eux par une force encore inconnue à l'époque. Seule l'atome d'hydrogène était une particule fondamentale, les autres atomes en étant simplement des dérivés. Mais cette hypothèse a fini par être mise en défaut suite à des mesures plus précises, ce qui réfuta l'idée de Prout. La proportionnalité entre masse atomique et masse de l'hydrogène était simplement approximative. Cette approximation a d'ailleurs été nommée règle de Prout en son honneur.
Grâce à Prout et quelques autres scientifiques, les chimistes prirent l'habitude de mesurer la masse d'un atome par rapport à la masse de l'hydrogène. Par exemple, le Carbone a une masse égale à 12 atomes d'hydrogène, l'Oxygène 8 fois, etc. Le coefficient de proportionnalité est appelé le nombre de masse, noté A. Par exemple, le nombre de masse du Carbone est de 12 (A = 12), celui de l'oxygène 8, etc. Les chimistes utilisaient aussi le nombre atomique Z, qui indique la position de l’élément chimique dans le tableau périodique de Mendeleïev. Certaines relations entre Z et A laissaient penser que le noyau n'est pas d'un seul tenant et donnent des indices sur ce qui se trouve à l'intérieur d'un atome.
- Les chimistes ont remarqué que le nombre de masse est approximativement égal au double du nombre atomique : .
- Un même élément chimique correspond à plusieurs formes de Z identique, mais de A très différents. Ces formes alternatives d'un même élément chimique, qui sont plus lourdes ou plus légères que l’élément normal, sont appelées des isotopes.
Par la suite, on découvrit le phénomène de radioactivité alpha, où un atome émet spontanément une particule dite alpha. Cette particule alpha a un nombre de masse égal à 4, soit quatre atomes d'hydrogènes et un Z égal à 2. Il s'agit donc d'Hélium, et plus précisément d'un de ses isotopes, nommé Hélium-4 (la forme la plus courante de l'Hélium). En 1911, le physicien Rutherford supposa que tous les atomes sont composés de particules alpha, donc de noyaux d'Hélium-4. La supposition de Rutherford permettait d'expliquer le fait que pour tous les atomes, les particules alpha comprises. Mais elle collait mal avec deux observations. Déjà, la moitié des atomes ont un Z impair, ce qui ne colle pas avec de l'Hélium ayant un Z pair. Ensuite, certains atomes lourds ne respectent pas la formule et ont un nombre de masse légèrement plus grand que 2 Z. Cet excès de A ne colle pas avec un atome composé de particules alpha et encore moins avec un atome composé d'hydrogène. On pourrait cependant pu sauver l'hypothèse en remplaçant les particules alpha par le noyau d'hydrogène pour qui , comme de nombreux chimistes l'avaient pensé auparavant, mais cela n'expliquait pas l'existence des isotopes et était incompatible avec l'approximation .
Les modèles de l'atome suite à la découverte de l'électron
[modifier | modifier le wikicode]La science fît un grand bond en avant suite à la découverte de l'électron, une particule chargée négativement et de faible masse. C'est alors que commença la découverte de la structure atomique, qui mena finalement à la découverte du noyau atomique. Les savants découvrirent que l'atome n'est pas une entité élémentaire, mais qu'il est composé de plusieurs particules individuelles, dont les électrons, qui s'assemblent pour former un atome. Thomson, qui avait découvert l'électron en 1903, a rapidement deviné que l'atome contient des électrons. Mais les électrons sont des particules chargées négativement, alors que les atomes sont neutres : l'atome doit contenir des charges positives pour compenser la charge électronique. Plusieurs modèles concurrents apparurent alors.
Dès 1903, Philipp Lenard supposait que les charges des électrons étaient compensées par des particules chargées positivement. Il avait établi un modèle où chaque électron était lié par des interactions électrostatiques à une particule positive. L'ensemble était neutre et il était logique que des charges opposées s'attirent au point de se lier. Mais il fallait expliquer pourquoi chaque couple électron-particule s'assemblait pour former un noyau. Les forces électrostatiques auraient pu servir à cela, mais les calculs ne collaient pas à certaines observations.
Thomson, quant à lui, supposa que les électrons sont noyés dans une sorte de gelée chargée positivement, chose qui a été décrit comme des raisins dans du pudding. Les électrons étaient, dans ce modèle, libres de se déplacer dans la gelée positive, leur trajectoire étant grossièrement elliptique, mais très irrégulière. Les électrons ont peu de chances de quitter l'atome, du moins, sans qu'on leur apporte d'énergie. Si un électron s'éloigne trop du centre, la répartition des charges se déséquilibre et fait naître une charge positive au centre de l'atome. La charge induite attire alors l’électron fugueur vers le centre de l'atome, ce qui l'empêche de fuir. Thomson compris rapidement que la trajectoire des électrons avait un lien avec le phénomène des raies atomiques, mais ne put le démontrer formellement. Il fallut attendre le modèle de Bohr pour que ce lien devienne plus clair. Mais laissons cela à un cours de chimie.
En 1904, le scientifique japonais Hantarō Nagaoka proposa un modèle alternatif à celui de Thomson. Il considérait que celui-ci était incorrect, pour diverses raisons, la principale étant que des charges opposées en peuvent pas s'interpénétrer (ce qui est le cas dans le modèle de Thomson). Son modèle de l'atome était basé sur le fait que la charge positive était localisée au centre de l'atome, dans un petit espace : le noyau atomique. Les électrons tournaient autour du noyau atomique, sur des orbites elliptiques ou circulaires. La ressemblance de cette configuration fait que sa théorie a été appelée le modèle planétaire de l'atome. Il supposait que le noyau était très massif comparé aux électrons, afin de garantir la stabilité de l'ensemble. Les électrons étaient maintenus sur leurs orbites par les forces électrostatiques, à savoir l'attraction du noyau positif. Ces deux prédictions furent confirmées par la suite, mais divers éléments plus précis du modèle furent cependant réfutés par la suite. Le modèle exact était correct dans les grandes lignes, mais ses détails et sa formulation mathématique avaient quelques soucis sur lesquels nous ne nous attarderons pas.
 |
 |
 |
La découverte du noyau : l'expérience de Rutherford-Geiger-Mardsen
[modifier | modifier le wikicode]L'existence du noyau postulé par Hantarō Nagaoka fût confirmée en 1909 par l'expérience de Rutherford-Geiger-Marsden., réalisée par deux expérimentateurs, Hans Geiger et Ernest Marsden, sous la direction d'Ernest Rutherford. Cette expérience visait à étudier la répartition des constituants de l'atome en bombardant une feuille d'or par un faisceau de particules alpha. Elles auraient alors dû traverser l'atome sans interagir avec les électrons et ses autres constituants. Pour vérifier le comportement des particules alpha, un écran sensible était placé derrière la feuille d'or. Quand une particule alpha touchait l'écran, un point lumineux s'affichait sur celui-ci.
Les scientifiques s'attendaient à ce que la feuille soit globalement transparente aux particules alpha, ne laissant qu'un faisceau très fin sur l'écran. Mais ils virent que le faisceau se dispersait, avec des points étalés sur de grandes distances. Les particules alpha rebondissaient sur l'atome, pourtant presque vide. Les expérimentateurs purent montrer que 0,01 % des particules étaient déviées, les 99,99 % autres traversant la feuille d'or sans encombre. Les angles de déviation étaient assez variés et certaines particules étaient même renvoyées en arrière. Rutherford décrit ce résultat en ces termes : « tout se passe comme si vous bombardiez une feuille de papier avec un obus de 15 pouces, que le projectile rebondisse vers vous et vous touche ». Il devait y avoir quelque chose dans l'atome sur lequel les particules rebondissaient, mais quoi ?


Le problème principal était que certaines particules rebondissaient avec un angle de plus de 90°. Les règles de la mécanique, appliquées aux collisions entre deux corps, nous disent que cela n'est possible que si l'impacteur est plus léger que le corps impacté. La seule explication au rebond des particules alpha est donc qu'elles cognent sur quelque chose de plus lourd qu'elles. Mais les électrons sont bien plus légers que les particules alpha, ce qui fait qu'il doit y avoir autre chose dans l'atome... Le faible nombre de particules renvoyées donne quelques contraintes sur la taille de cet autre chose : il doit être très petit. Plus cet objet massif est gros, plus les particules alpha ont de chances de cogner dessus et plus il devrait y en avoir qui rebondissent vers l'arrière. Le faible nombre de particules alpha renvoyées implique que c'est un petit objet, à peine un pourcent du volume de l'atome, voir moins. En clair : l'atome contient un petit objet très petit mais très massif, vraisemblablement de charge positive.
Rutherford établi alors une formule qui relie le pourcentage de particules qui rebondissent avec un angle de rebond . Nous la démontrerons dans le chapitre sur les diffusions nucléaires et l'étudierons plus en détail. Pour le moment, contentons-nous de dire qu'elle suppose ceci : la particule alpha ne rebondit pas vraiment sur le noyau, mais est en réalité repoussée par répulsion électrostatique. Cette répulsion dévie la particule et peut même la renvoyer si elle arrive avec la bonne trajectoire. La formule de Rutherford collait parfaitement avec les résultats de ses assistants, sauf pour des valeurs d'angle particulièrement élevées. Ils ne le savaient pas à l'époque, mais ces déviations entre formule de Rutherford et résultats permettent d'étudier la structure interne du noyau. Mais revenons à nos moutons... Rutherford utilisa cette formule pour calculer la taille du noyau et l'appliqua sur les expériences de ses assistants. Il put ainsi déterminer la taille du noyau atomique, qui se révéla extrêmement petite. Le noyau ne fait que 1% du volume de l'atome, alors qu'il concentre la majorité de sa masse. Environ 99% de l'atome est intégralement composé de vide, électrons et noyau compris.
La découverte du proton
[modifier | modifier le wikicode]Après la découverte du noyau, les physiciens ont établi que le noyau était chargé positivement et de petite taille. Sa charge est de plus égale à la charge des électrons, mais de signe contraire. Certains scientifiques supposèrent que le noyau était lui-même composé de particules élémentaires, chargées positivement et de même masse que le noyau d'hydrogène. Parmi ces raisons, on peut citer la règle de Prout, mais celle-ci est loin d'être la seule. Antonius van den Broek a supposé que la place de chaque élément dans la classification périodique est égale à la charge de son noyau, ce qui est confirmé par les expériences d'Henry Moseley en 1913.
La découverte du proton
[modifier | modifier le wikicode]En 1919, Rutherford fit une nouvelle expérience qui lui permit de découvrir le premier composant du noyau. Il voulait vérifier les résultats d'une expérience de Mardsen, qui avait observé l'émission d'hydrogène lors de la désintégration du Radium. Mardsen avait observé l'émission de particules alpha d'un morceau de radon dans une chambre remplie d'Hydrogène gazeux. Les particules alpha émises entraient en collision avec des atomes d'Hydrogène, les envoyant sur un écran scintillant (comme dans l'expérience de Rutherford, sauf que l'écran était sensible aux atomes d'Hydrogène). Il observait bien des points scintillants quand la chambre était remplie d'Hydrogène, preuve que le dispositif marchait parfaitement. Mais, quand il vida la chambre et la remplit d'air, il vit que des points scintillants apparaissaient toujours, bien que moins souvent. Il en déduit, on sait aujourd'hui à tort, que le radon émettait de l'Hydrogène.
Pour en avoir le cœur net, Rutherford répliqua l'expérience en remplaçant l'Hydrogène par du dioxyde de Carbone, de l'Oxygène et de l'air sec. Seul l'air sec permettait d'observer ce phénomène, ce qui fit penser à Rutherford qu'il devait être lié à un gaz présent dans l'air qui n'est ni CO2 ni O2 : l'Azote. Pour le vérifier, Ruthetford bombarda des noyaux d'Azote avec des particules alpha très énergétiques. Il observa alors les scintillations, prouvant son hypothèse. Pour résumer, Rutherford pensait que les collisions entre particules alpha et Azote arrachaient des noyaux d'Hydrogène à l'Azote. Ce fût confirmé par des expériences dans des chambres à brouillards, qui permettent de voir les trajectoires des particules, qui donnaient des résultats compatibles avec l'hypothèse de Rutherford. Cette expérience montra que les noyaux peuvent se casser, suite à un choc ou spontanément, en émettant un noyau d'Hydrogène.
Les modèles du noyau avec électrons intranucléaires
[modifier | modifier le wikicode]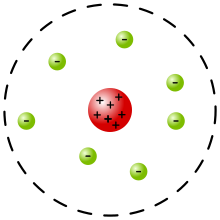
Preuve était faite que les noyaux contiennent des noyaux d'Hydrogène, qui sont composés d'une unique particule encore inconnue à l'époque : le proton. Les protons sont des particules chargées électriquement. Leur charge est positive, de même valeur absolue que celle de l’électron. Il a une masse de kg, ce qui est presque égal à 1836,15 fois celle de l’électron. La masse du noyau semble approximativement proportionnelle à la masse du proton. L'expérience de Rutherford montrait que le noyau contenait des protons et il était naturel de supposer qu'il était composé uniquement de protons. C'est d'ailleurs à la suite de ces découvertes que Rutherford proposa, en 1920, un modèle de l'atome similaire au modèle de Nagaoka (qu'il cite dans son article), mais sans ses défauts.
Mais cette hypothèse a un défaut : elle ne rend pas compte de la charge du noyau. En effet, si on suppose que le noyau atomique est composé de protons, alors la charge calculée ne correspond pas. Si on mesure la masse en unité d'atomes d'hydrogène et la charge électrique, il y a un facteur 2 entre ces deux valeurs : il doit y avoir deux fois plus de protons que d’électrons du point de vue de la masse, mais autant de protons que d’électrons du point de vue de la charge. Prenons l'exemple de l'atome de carbone 12, qui contient 6 électrons : son noyau a une charge de 6 (ce qui correspond à 6 protons), mais sa masse est de 12 fois celle du proton. Et ce problème se rencontre pour tous les noyaux, excepté pour l'hydrogène (et plus précisément pour son isotope appelé le protium). Pour résoudre ce problème, les physiciens ont postulé que le noyau contenait des électrons qui compensaient la charge de la moitié des protons. Cette théorie des électrons nucléaires avait cependant de nombreux problèmes techniques et expliquait mal certaines données expérimentales.
La découverte du neutron
[modifier | modifier le wikicode]La découverte du neutron en 1932 par Chadwick changea la donne. Les scientifiques ont rapidement compris que le noyau contenait à la fois des protons et des neutrons, suite à diverses observations qui montrèrent que le neutron est un constituant du noyau. Le neutron a une charge électrique nulle, contrairement au proton et à l’électron. Sa masse est très légèrement supérieure à celle du proton (un neutron est 1,0014 fois plus lourd que le proton) et vaut kg.
Les modèles ultérieurs de l'atome
[modifier | modifier le wikicode]Par la suite, les physiciens ont inventé d'autres théories de la structure atomique, mais celles-ci ne nous intéressent pas dans ce cours. Le fait est qu'elles se préoccupent presque uniquement du cortège électronique, à savoir l'ensemble des électrons d'un atome. Les plus connues sont le modèle de Bohr et de Schrödinger : elles se basent sur la physique quantique, ce qui les rend assez difficiles à comprendre pour le profane. Ceux qui veulent en savoir plus peuvent lire le Wikilivre suivant, qui détaille les différents modèles de l'atome. Mais nous n'en aurons pas vraiment l'utilité dans ce qui suit.






