Neurosciences/La migration des neurones neoformés
Dans le chapitre précédent, nous avons parlé de la neurogenèse, la création des nouveaux neurones. Dans ce chapitre, nous allons voir ce qu'il advient des neurones nouvellement formés. En théorie, les neurones pourraient rester en place une fois nés. Il leur suffirait de s'intégrer dans les réseaux neuraux existants en tissant des synapses avec leurs voisins immédiats. Mais les neurones ne peuvent pas s'accumuler sur leur lieu de naissance : au pire ils sont repoussés mécaniquement par de nouveaux venus, au pire ils doivent migrer activement. En dehors de quelques exceptions, ils sont programmés pour la seconde solution. Les neurones néo-formés vont se déplacer vers leur localisation finale. Ce processus de migration est le sujet de ce chapitre. Nous allons voir ce qu'il advient des neurones formés dans la crête neurale, puis de ceux du tube neural. Nous allons voir comment ils se déplacent, quels sont les mécanismes qui leur permettent de bouger, de trouver leur chemin, de savoir qu'ils sont arrivés à bon port.
La migration dans le système nerveux central
[modifier | modifier le wikicode]Dans le système nerveux central, la migration est le fait de processus complètement différents de ceux vus pour la crête neurale. Pour rappel, les neurones naissent dans deux zones principales lors du développement : la zone ventriculaire et la zone subventriculaire. Les processus de migration sont différents selon que les neurones quittent la zone ventriculaire ou la zone subventriculaire. Les neurones de la zone ventriculaire donnent naissance au cortex et à presque tout le reste du cerveau. À l'opposé, la zone subventriculaire ne forme qu'une poignée de neurones, localisés dans le bulbe olfactif. Et le chemin suivi par les neurones est différent. Mais dans les deux cas, les neurones sont guidés d'une manière ou d'une autre pour arriver à destination. Les neurones sont placés sur des tubes, qui servent de monorails cylindriques, qui emmènent les neurones à destination par translation sur le tube. Les tubes en question sont composés de cellules gliales. La différence est que dans le système nerveux, chaque tube est produit par un astrocyte unique, là où les tubes qui sortent de la crête neurale sont formés par agglomération de plusieurs astrocytes.
La migration à partir de la zone ventriculaire (migration radiale)
[modifier | modifier le wikicode]
1 : Zone ventriculaire (VZ pour Ventricular Zone en anglais)
2 : Plaque corticale (CP pour Cortical Plate en anglais.
Les neurones du système nerveux central sont formés dans la zone ventriculaire, et migrent à partir celle-ci. La zone ventriculaire contient des sortes de tubes posés à la verticale, qui servent de rail pour guider les neurones. Les neurones se déplacent sur la surface de ces tubes, jusqu’à leur position finale dans le système nerveux. Les tubes en question sont appelés les piliers de Corti. Ils ont une forme de T, dont la barre verticale sort de la zone ventriculaire et où la barre horizontale est placée au-dessous des méninges. Ils sont produits par des cellules gliales, des astrocytes pour être plus fin. Les cellules gliales à l'origine de ces tubes sont appelées des cellules gliales radiales, et sont des astrocytes un peu spéciaux. Les neurones vont s'accoler sur la barre verticale de ce T et remonter progressivement jusqu’à leur position finale.
Avant le démarrage de la migration, l'espace entre les méninges et la zone ventriculaire est organisé en plusieurs couches, que traverse la barre en T. Dans les grandes lignes, on trouve trois couches principales, elles-mêmes subdivisées en plusieurs sous-couches. La première couche est la zone ventriculaire qui contient les cellules-souches. La seconde couche est la couche du manteau, dans laquelle les neurones néoformés migrent vers leur destination finale. La troisième couche, la couche marginale, est le lieu où se développe la substance blanche des neurones. Ces trois couches auront un destin différent. La couche ventriculaire va perdre sa capacité de neurogenèse et se remplir d'épendymocytes : elle donnera la paroi des ventricules. La couche du manteau va se remplir de neurones qui donneront le néocortex. Enfin, la couche marginale va se remplir d'axones et deviendra la substance blanche du cerveau et/ou de la moelle épinière.
Le démarrage de la migration impacte l'organisation du tube neurale, en faisant apparaître d'autres couches que les trois couches initiales. La couche marginale se remplit de substance blanche et se subdivise en deux couches. Sous les méninges, on trouve une couche de laminine, dans laquelle s'étalent les barres horizontales des tubes en T. Juste en dessous, on trouve une couche de réeline, dans laquelle des cellules de Cajal-Retzius produisent de la réeline, une protéine spéciale qui arrête les neurones lors de leur migration. La réeline stoppe la migration des neurones, elle leur indique qu'il faut qu'ils arrêtent leur progression et se fixent. La couche centrale, appelée la couche du manteau est initialement vide. Par la suite, elle va se remplir de piliers de Corti, sur lesquels les neurones vont migrer. Les neurones vont s'accumuler sur la face interne de la couche marginale et donne naissance à la plaque corticale, qui donnera naissance au cortex cérébral. En dessous de la plaque corticale, on trouve une petite couche sous-corticale, qui donnera naissance aux structures sous-corticales et à quelques noyaux. Enfin, on trouve la couche intermédiaire proprement dit, dans laquelle les neurones migrent vers la plaque corticale.

Vu ce qui vient d'être dit, on pourrait croire que les couches du cortex se forment de l'extérieur vers l'intérieur. D'abord la couche au contact des méninges se forme, puis une couche vient s’accoler en dessous, et ainsi de suite. Mais dans les faits, c'est l'inverse qui se passe. Rappelons que la migration des neurones est arrêtée par la couche de réeline, qui indique aux neurones qu'ils doivent s’arrêter. Sans elle, les neurones s'accumuleraient dans la couche marginale. Il faut savoir que les neurones migrants peuvent parfaitement traverser la plaque corticale et qu'ils n'ont aucune raison de ne pas le faire. Ce faisant, les neurones migrants traversent la plaque corticale, mais sont arrêtés par la couche de réeline. Les neurones vont donc s'insérer à la base de la couche marginale et vont repousser les couches précédentes, ce qui explique pourquoi les couches s'accumulent dans le "mauvais sens".
Avec ce qu'on vient de dire, on devine que l'absence de réeline entraine des troubles dans le développement du cortex. Divers expériences ont cherché à savoir ce qu'il en était. Pour cela, les chercheurs ont utilisé des souris mutantes, dans lesquelles la production de réeline est absente. Ils ont ensuite analysé leur cortex, une fois la souris suffisamment développée. Le résultat est que le cortex est complètement désorganisé et n'est pas structuré en couches comme il le devrait. Chez les fœtus mutants, la plaque corticale est désorganisée, sans compter que les cellules sous-corticales sont placées directement sous la couche marginale (et non sous la plaque corticale). La raison à cela est que les neurones migrants ne se sont pas arrêtés sous la couche marginale et n'ont pas pu former une succession de couches. À la place, les neurones se sont mélangés les uns avec les autres, donnant un résultat sans structure notable.
La migration à partir de la zone subventriculaire
[modifier | modifier le wikicode]
En plus de la neurogenèse de la zone ventriculaire, des neurones naissent dans la zone subventriculaire localisée juste au-dessus. Évidemment, les nouveaux neurones ne restent pas dans la zone subventriculaire, mais migrent vers le bulbe olfactif et quelques autres aires cérébrales proches. Une fois arrivés à destination, les neurones se différencient en cellules granulaires ou en neurones périglomérulaires, et restent en place une fois différenciés. Chez les rongeurs, le chemin par lequel les neurones migrent de la zone subventriculaire porte un nom : c'est le Rostral migratory stream pour les anglais, que l'on pourrait traduire par chemin de migration rostrale en français. Il n'existe pas tel quel chez les humains, mais il doit exister un chemin de migration similaire, bien que les structures anatomiques humaines doivent être différentes.
La migration via le Rostral migratory stream est assez particulière, unique en son genre. Contrairement à ce qu'on observe dans les autres formes de migration neuronale, les astrocytes jouent un rôle secondaire dans la migration des neurones hors de la zone subventriculaire. Ici, la migration est surtout guidée par les neurones eux-mêmes. Les neurones nouvellement formés s'accrochent aux neurones déjà en route, chaque neurone sert de guide au suivant. Le tout forme une chaine de neurones qui part de la zone subventriculaire et arrive à destination. Ce mode original de migration est appelé assez sobrement de chaine de migration. Les astrocytes servent de tissu de soutien et évitent que les neurones quittent la chaine, mais ils n'en sont pas à l'origine. La capacité qu'ont les neurones à s'attacher en chaine est dépendante de la présence d'intégrine , une molécule qui permet aux neurones de s'accrocher les uns aux autres. Formellement, il s'agit d'une molécule d'adhésion cellulaire, une protéine qui permet à deux cellules de se coller l'une à l'autre, de se joindre l'une à l'autre.
En outre, les neurones sont guidés dans leur déplacement par des molécules qui attirent les neurones dans la bonne direction, ou au contraire les repoussent. Parmi les molécules chimio-attractrices, on peut citer la netrin-1 et la glial cell line derived neurotrophic factor. Pour les molécules qui repoussent les neurones, on peut citer les molécules slit-1 et slit-2. Divers récepteurs de la tyrosine-kinase de famille Eph ont aussi un rôle à jouer dans ce processus.
La migration des cellules de la crête neurale
[modifier | modifier le wikicode]Pour rappel, les cellules du tube neural vont donner le système nerveux central, tandis que celles de la crête neurale (une crête de cellules qui surmonte le tube neural) vont donner le système nerveux périphérique et d'autres structures anatomiques. Plus précisément, la crête neurale donne naissance : aux mélanocytes de la peau, à du cartilage crânien, au système nerveux périphérique du tronc, à une partie de la glande surrénale, la medulla. Les cellules de la crête neurale doivent donc se déplacer pour se répartir dans le corps tout entier, pour donner des nerfs et d'autres structures.
Le détachement des neurones migrants
[modifier | modifier le wikicode]Pour migrer, les cellules de la crête neurale doivent se détacher de leurs voisines. La crête neurale est en effet un tissu épithélial, c'est à dire une couche de cellules collées ensembles, jointives. Les cellules de ce genre de tissus sont jointes par des protéines d’adhésion cellulaire assez variées : de la Cadherine, de la fibronectine, et bien d'autres. Le tissu épithélial est séparé du reste du corps par une lame basale, aussi appelée membrane basale. La couche de cellules épithéliale repose au-dessus ou au-dessous de la lame basale. Le côté des cellules en contact avec la lame basale est appelé le pôle basal, alors que l'autre est appelé le pôle apical.


Pour se détacher, les cellules doivent faire deux choses : couper les liens qu'elles ont avec leurs voisines, et se détacher de la lame basale. Pour le premier, elles doivent éliminer les protéines d'adhésion cellulaires qui les font coller à l'épithélium. Rappelons que ces protéines se lient entre elles, un peu comme du scratch ou du velcro, ce qui demande aux deux cellules jointives d'exprimer des molécules adhésives. Pour bien visualiser le tout, imaginez ce qui se passerait si on plaquait du scratch sur un sol lisse : cela ne collerait pas. C'est la même chose pour les cellules : si elles éliminent leur "scratch moléculaire", elles ne collent plus à leurs voisines, quand bien même celle-ci sont encore adhérentes. Pour se détacher de la lame basale, les cellules vont produire de quoi dégrader celle-ci, de quoi la digérer localement. La lame basale va alors disparaître aux bords de la cellule productrice, qui pourra s'en détacher. Les deux processus sont illustrés ci-contre.
Ces deux processus, détachement de leurs voisines et digestion de la lame basale, sont gouvernés par la génétique. Les cellules de la lame basale sont programmées pour se détacher ainsi, en réaction à un signal moléculaire. Le processus est courant dans de nombreux tissus et le tissu nerveux ne fait pas exception. On sait que la protéine slug est impliquée dans ce processus que nous ne détaillerons pas plus que cela. La migration semble induite par diverses molécules, et notamment les BMPs, avec une influence mineure des WNTs, des FGFs, de l'acide rétinoïque, et autres facteurs de transcription courants. Par contre, la protéine SHH aurait un effet inhibiteur sur la migration. Remarquons que les facteurs de transcription favorisant la migration sont produits au niveau dorsal (là où se trouve la crête neurale), alors que l'inhibiteur est produit au niveau ventral. Toujours est-il que ce processus de détachement se propage sur la crête neurale, dans le sens pied-tête. Il commence au niveau rostral et se propage vers l'extrémité caudale, c'est à dire des pieds vers la tête.
L'adhésion au tissu conjonctif
[modifier | modifier le wikicode]Une fois qu'elles ont quitté le tissu épithélial, les futurs neurones se déplacent dans un autre genre de tissu : du tissu conjonctif. Celui est composé de cellules qui sont englobées dans un lâche amas de protéines, la matrice extracellulaire. Les cellules adhèrent à la matrice extracellulaire en se fixant sur ses protéines. Pour cela, elles disposent de protéines d’adhésion cellulaires qui se collent à la matrice extracellulaire. Ces molécules sont différentes des protéines d'adhésion épithéliales. Dans l'épithélium de la crête neurale, les protéines d'adhésion étaient surtout de la classe des cadhérines. Mais dans le tissu conjonctif, les cadhérines disparaissent et laissent la place à du collagène, de la fibronectine et d'autres molécules. Les futurs neurones s'adaptent en sécrétant de quoi s'accrocher au collagène, à la fibronectine, à l'intégrine, et aux autres protéines du genre.
Sur leur chemin, les cellules vont être soumises à différentes substances chimiques, qui les forceront à se spécialiser en récepteur sensoriel, en neurone de ganglion spinal, etc. Une fois arrivé à destination, les futurs neurones se fixent et ne bougent plus. Évidemment, quelque chose leur dit quand s’arrêter, les neurones ne se dispersant pas aléatoirement dans tout le corps. Mais à l'heure actuelle, on ne sait pas grand-chose sur ce mécanisme, qui reste encore mystérieux. On suppose que les neurones se détachent de la matrice extracellulaire et se condensent en ganglions, à l’exception de ceux qui se répartissent en dehors des ganglions. De la même manière, on sait encore peu de choses sur ce qui guide les cellules vers leur destination finale, ce qui les garde sur le bon chemin.
La spécialisation régionale
[modifier | modifier le wikicode]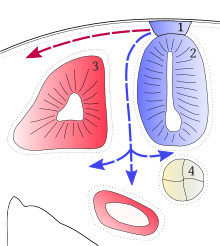
1 : Crête neurale.
2 : Tube neural.
3 : Somites.
4 : Notochorde (future colonne vertébrale).
Le mouvement des cellules de la crête neurale sont indiqués dans le schéma ci-contre. On voit qu'il y a deux chemins de migration : un premier juste passe en dessous de l'ectoderme, et un autre qui s'enfonce et contourne les somites. Le premier chemin est que prennent les cellules qui donneront les mélanocytes et le squelette. Le chemin profond, quant à lui, est celui qui donne naissance au système nerveux périphérique et à la glande surrénale (sa médulla pour être précis).
Le destin d'une cellule de la crête neurale dépend de sa position. Par exemple, les cellules situées dans le bas du dos vont se répartir dans le bas du corps, celles situées proches du futur visage vont se répartir dans le corps, etc. Dans les grandes lignes, on peut distinguer quatre zones de la crête neurale, qui auront des destinées différentes : une zone crânienne, une zone vagale, une zone thoracique et une zone lombaire-sacrée.
- Les cellules de la zone crânienne donneront les nerfs crâniens, à quelques exceptions près. Elles formeront les ganglions sensoriels crâniens, le ganglion parasympathique qui innerve les yeux, et du cartilage facial.
- Les cellules de la zone vagale ne donneront pas le nerf vague, malgré ce que laisse penser leur nom, mais le système nerveux entérique. Tout défaut de formation de la zone vagale entraîne l'absence de système nerveux entérique. Les scientifiques ont observé chez certaines souris que des mutations peuvent faire disparaître la crête neurale dans sa portion vagale. En conséquence, leur colon n'est pas envahi par les cellules nerveuses entériques. Le résultat est que le colon ne peut pas bouger, du moins dans la portion où il n'y a pas de cellules nerveuses entériques. Il existe une maladie similaire chez l'humain, qui s'appelle la maladie de Hirschsprung, qui a une cause similaire.
- les cellules de la zone thoracique donnent naissance aux mélanocytes de la peau, ou alors au système nerveux périphérique du tronc. Elles forment notamment les ganglions sympathiques, les ganglions spinaux, mais aussi les cellules de la médulla des surrénales. De plus, elles forment les cellules gliales du système nerveux périphérique du tronc, à savoir les cellules de Schwann.
La spécialisation des neurones dépend surtout de la position de départ des cellules. Cela peut se prouver par des expériences de greffe neurale, dans laquelle on prend un morceau de la crête neurale, qu'on déplace dans une autre zone. Les expérimentateurs ont juste à regarder ce qu'il advient des neurones de la zone greffée. On peut alors faire face à plusieurs situations : soit les neurones greffés meurent, soit ils se spécialisent comme leurs voisins, soit ils se spécialisent comme les neurones de la zone d'où ils ont été retirés. La différence est ce qui programme la spécialisation : induite par l'environnement dans le second cas, induite dans la crête neurale dans le dernier. Si la cellule est programmée dans la crête neurale pour devenir un neurone sensoriel, alors le greffer ailleurs n'y changera rien. Inversement, si la programmation intervient plus tard, une fois que le neurone a migré, la greffe devrait laisser le neurone évoluer comme ses voisins. Dans le cas où le neurone évolue comme ses voisins, en fonction de son environnement, on dit que la spécialisation des neurones dépend de leur position. Dans le cas où la position dans la crête neurale programme sa destinée, on parle de spécialisation par détermination axiale.
Le résultat des expériences de greffe est assez variable selon la zone choisie. Dans tous les cas, les neurones migrent vers l'endroit spécifié par leur position : une cellule placée dans la zone crânienne migre vers le crane, celles dans la zone thoracique vers le tronc, etc. Dans la plupart des cas, elles vont se spécialiser en neurones qui sont identiques à leurs voisins immédiats : par exemple, une cellule qui migre dans la peau se spécialisera en neurone sensoriel du toucher, pas en neurone de ganglion sympathique. La spécialisation des neurones dépend donc de leur environnement après migration, mais pas de leur position initiale dans la crête neurale. Mais il existe quelques exceptions qui prouvent que les deux mécanismes de programmation, axiale et environnementale, sont à l’œuvre.



