Neurosciences/Le développement du système nerveux
Le système nerveux d'un animal est une petite merveille de la nature, qui nécessite l'intervention de nombreux processus très contrôlés pour se former. La formation du système nerveux commence très rapidement, alors que l'enfant est encore dans le ventre de sa mère. Tout commence peu après la conception, dès la troisième semaine après la formation de l’œuf (l'ovule fécondé, pour rappel). Par la suite différents processus vont s’enchaîner pour former l'ébauche du système nerveux. Le cerveau et la moelle épinière vont se former, le cerveau va se plisser, des neurones vont se développer, etc. Et cela continue même après la naissance : le cerveau continue de se développer lors de l'enfance, et même lors de l'adolescence. Ce n'est qu'une fois atteint la vingtaine d'années que le système nerveux est plus ou moins stabilisé, même si le vieillissement finit par se faire sentir lors du grand âge. Ce chapitre va expliquer comment ces processus se déroulent, comment ils s’enchaînent.
La formation du système nerveux
[modifier | modifier le wikicode]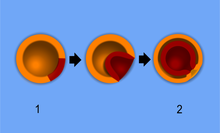
Nous allons commencer l'abord du développement du système nerveux après que l’ovule soit fécondé. Celui-ci commence alors à se diviser de plus en plus, passant d'une cellule à 2, puis 4, et ainsi de suite jusqu’à 64 : à ce stade l'embryon est ce qu'on appelle une morula, un simple amas de cellules. Par la suite, ces cellules s'organisent : elles forment une couche de cellules qui entoure une sphère pleine d'eau, le blastocyste. Ensuite, le blastocyste s'invagine vers l'intérieur, ce qui fait que le blastocyste se retrouve avec deux couches : l'endoderme à la surface de la sphère et l’ectoderme à l'intérieur. Entre les deux couches, on trouve un vide qui évoluera en se remplissant de cellules : le mésoderme. C'est à ce moment que plusieurs étapes vont se succéder, pour former la première ébauche de système nerveux. Ces étapes sont résumées dans le tableau ci-dessous. Nous allons les détailler dans ce qui suit.
| Étape | Description | Temps écoulé depuis la conception |
|---|---|---|
| Neurulation | Individualisation des premiers tissus nerveux. | Entre 3 et 4 semaines. |
| Régionalisation | Subdivision du système nerveux en aires distinctes. | Entre 5 et 10 semaines. |
| Développement du cortex | Formation des couches du cortex. | À partir de la 7ème semaine. |
| Synaptogenèse | Formation des premières synapses et augmentation de leur nombre. | Entre 30 semaines et 2 ans. |
- Cette section décrit le développement embryonnaire du système nerveux des déutérostomiens uniquement, et plus précisément des vertébrés. Il ne tente pas de décrire le développement du système nerveux des organismes plus simples, comme les vers plats, les annélides, les céphalopodes, les arthropodes et autres. Cela ne signifie pas que les scientifiques n'ont pas étudié la formation du système nerveux de ces animaux, des exemples comme l'aplysie ou certains vers du clade C.Elegans suffisant à prouver le contraire. Mais nous ne parlerons pas de ces résultats dans cette section.
La neurulation
[modifier | modifier le wikicode]C'est suite à la gastrulation que se forme la première ébauche de système nerveux, via un processus dit de neurulation. La neurulation se déroule en plusieurs étapes distinctes nommées neuralisation, invagination, fermeture du tube neural et migration.
- Neuralisation : Lors de cette phase, une portion de l'ectoderme commence à se transformer en tissu nerveux. Cette zone va prendre la forme d'une plaque neurale, localisée à l'endroit où la colonne vertébrale se situera une fois l'embryon grandit.
- Formation de la gouttière neurale : Une fois mise en place, cette plaque va diminuer d'épaisseur. Une fois cet amincissement terminé, l'ensemble forme une gouttière neurale, entourée par des crêtes neurales.
- Fermeture du tube neural : À la troisième étape, la gouttière se plie sur elle-même au point que les deux crêtes se soudent les unes aux autres. La plaque neurale se referme sur elle-même, et forme un tube : le tube neural.
- migration : Les cellules du tube neural et de la crête neurale vont migrer vers leur position définitive.

La neuralisation
[modifier | modifier le wikicode]Les cellules de la plaque neurale sont des cellules de l'ectoderme, qui peuvent se transformer lors du développement, soit en épiderme (la peau), soit en tissu neural. En-dehors de la plaque neurale, l’ectoderme se transforme en peau. Mais dans la plaque neurale, les cellules se transforment en neurones et en cellules gliales. Cette spécialisation est gouvernée par la présence ou l'absence de substances chimiques dans le tissu en cours de développement, ces dernières étant appelées des facteurs de différentiation. Sans facteurs de différentiation, le destin d'une cellule d'ectoderme est de devenir une cellule nerveuse. Dans ce qui deviendra la peau, les facteurs de différentiation poussent les cellules à se transformer en cellules de peau. Dans la plaque neurale, leur effet est annulé et les cellules se développent comme s'il n'y avait pas d'influence extérieure. Le tissu, qui échappe à la spécialisation en tissu dermal, devient du tissu neural.
Les facteurs de différentiation les plus importants dans ce processus sont des protéines produites lors du développement. Les molécules de la famille des bone morphogenetic proteins (BMPs) sont celles qui forcent le tissu ectodermal à se spécialiser en peau. Diverses expériences ont montré que si l'on supprime les BMPs dans un morceau de tissu ectodermal, il se spécialise en tissu nerveux. Par contre, la présence de BMPs dans ce même tissu le pousse à se transformer en peau, ongles et autres tissu épidermiques. Les inhibiteurs présents dans la plaque neurale sont assez nombreux, mais les plus connus sont les suivants : follistatin, noggin, chordin et Cerberus. Tous sont des antagonistes des récepteurs aux BMPs, ce qui fait qu'ils inhibent l'action des BMPs sur le tissu ectodermal. La voie de signalisation des BMPs et de ses antagonistes est celle qui a été le plus étudiée, mais les recherches se poursuivent sur le sujet et il n'est pas impossible que l'on découvre d'autres facteurs de différentiation neurale.

Les inhibiteurs des BMPs sont produits par la notochorde, une structure embryonnaire qui donnera la colonne vertébrale, placée juste en-dessous de la plaque neurale. Une fois produite dans la notochorde, les inhibiteurs se dispersent dans l'organisme, majoritairement en direction de l'ectoderme. Vu qu'ils se dispersent, leur concentration diminue avec la distance et ils n'ont plus d'effet au-delà d'une distance assez petite (quelques centimètres, millimètres). L'ectoderme de la future plaque neurale est suffisamment imbibé par les inhibiteurs des BMPs pour qu'ils agissent. À l'inverse, les autres portions de l'ectoderme ne sont pas assez riches en inhibiteurs pour qu'ils fassent effet. On comprend ainsi pourquoi la plaque neurale a une extension limitée, et surtout pourquoi elle se forme au niveau de la colonne vertébrale.
Le tube neural (description et évolution)
[modifier | modifier le wikicode]Après l'étape de neuralisation, la plaque neurale se replie et se referme sur elle-même. Le résultat est le tube neural, un tube "creux" dont les parois sont remplies d'ectoderme neural. De part sa forme, on se doute qu'il s'agit d'une ébauche de la moelle épinière, mais pas seulement. Le tube neural proprement dit donnera naissance au système nerveux central, aussi bien le cerveau que la moelle épinière. Le tube neural est séparé du reste du corps par deux membranes : une membrane limitante interne, et une membrane limitante externe. Entre ces deux membranes, on trouve un tissu neural en cours de développement. L'intérieur du tube neural, la lumière du tube neural se remplit de liquide céphalo-rachidien et donne le système ventriculaire, ainsi que les méninges.

Au bout de quatre semaines, le tissu du tube neural s'organise lui-même en plusieurs couches distinctes. En partant de l'intérieur vers l'extérieur, on distingue les trois couches suivantes :
- La première couche, la couche ventriculaire, aussi appelée la zone ventriculaire est une zone de fabrication de neurones.
- La seconde couche, la couche intermédiaire, contient les neurones fabriqués dans la zone ventriculaire qui ont migré vers l'extérieur.
- La troisième couche, la couche marginale, se remplit progressivement de la substance blanche.
La zone ventriculaire contient des cellules épendymaires, mais aussi des cellules souches neurales qui peuvent se différencier en cellules gliales et en neurones. On verra dans quelques chapitres qu'elle est la source principale de neurones dans le système nerveux : presque tous les neurones du cerveau sont fabriqués dans cette couche et migrent dans leur position définitive. Elle persiste durant un moment, mais régresse une fois que la production de nouveaux neurones est inutile et finit par disparaître.
La couche intermédiaire donnera la substance grise, alors que la couche marginale évolue en substance blanche. Cette structuration entre substance grise à l'intérieur et substance blanche à l'extérieur se retrouve aussi bien dans le cerveau que dans la moelle épinière.
Dans la moelle épinière et le tronc cérébral, on retrouve bien la substance grise au centre et la substance blanche vers l'extérieur. La seule subtilité est que la substance grise "se déforme" pour donner naissance aux cornes dorsales et ventrales, et acquiert une forme de papillon (quand on regarde la section). Dans le détail, les neurones formés dans la zone ventriculaire s'accumulent dans la couche du manteau au niveau de deux renflements : un renflement dorsal qui évoluera en cornes dorsales, et un renflement ventral qui donnera les cornes ventrales. Quant à la lumière du tube neurale, elle deviendra de plus en plus étroite et donnera finalement le canal épendymaire, le canal central dans lequel circule le liquide céphalo-rachidien.
Dans le tronc cérébral, les plaques alaires et basales se subdivisent ensuite pour former plusieurs colonnes, qui donneront elles-mêmes naissance aux noyaux du tronc cérébral. Mais nous verrons cela en détail dans la suite du chapitre, dans la section sur le développement du tronc cérébral.
En dehors du tronc cérébral et de la moelle épinière, la structuration en plaque alaire et basale n'existe pas et une organisation bien plus complexe voit le jour. Le cerveau antérieur et le cervelet ne gardent pas de trace de l'organisation en plaque alaire et plaque basale. Au niveau embryologique, le tronc cérébral ressemble donc à un prolongement de la moelle épinière, contrairement au reste du cerveau. Cela fait que le cervelet et le cerveau antérieur sont regroupés dans les centres supérieurs, qui ne conservent pas l'organisation simple de la moelle épinière. Il y a donc absence de plaque basale dans les centres supérieurs, avec aussi une quasi-absence de plaque alaire.
Néanmoins, il existe bien une plaque alaire dans le prosencéphale, mais pas de plaque basale. La plaque alaire du prosencéphale est divisée en une portion ventrale et une portion dorsale par le sillon hypothalamique. Ce sillon est composé d'un creux entouré de deux renflements, le celui sur la portion ventrale étant appelé le renflement hypothalamique, celui sur la portion dorsale étant appelé le renflement thalamique. Comme leurs noms l'indiquent, le renflement hypothalamique donne naissance à l'hypothalamus, alors que le renflement thalamique donne naissance au thalamus. Un autre renflement de plus petite taille donne naissance à l'épithalamus, avec la glande pinéale.
La migration neuronale
[modifier | modifier le wikicode]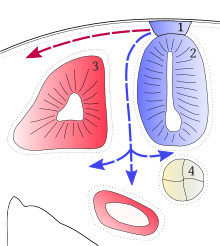
1 : Crête neurale.
2 : Tube neural.
3 : Somites.
4 : Notochorde (future colonne vertébrale).
Parlons maintenant de la dernière étape, l'étape de migration, la dernière étape qui a lieu une fois le tube neural fermé. Lors de cette étape, les cellules du tube et de la crête neurale vont se déplacer vers leur position définitive. Le tube neural et la crête neurale donneront naissance à deux subdivisions différentes du système nerveux. Le premier donne naissance au système nerveux central à savoir le cerveau et à la moelle épinière. Les neurones de la crête neurale vont se regrouper pour former le système nerveux périphérique, à savoir les nerfs et ganglions spinaux. Pour être plus précis, ils vont donner naissance au système nerveux périphérique du tronc, système nerveux autonome compris, mais aussi à une partie de la glande surrénale. Ils vont aussi donner naissance à d'autres tissus, sans rapport avec le système nerveux. Par exemple, ils vont se métamorphoser en mélanocytes (les cellules qui colorent la peau et font bronzer), ainsi qu'en tissu squelettique.
Les cellules du tube neural sont presque en place et n'ont pas tellement à se déplacer. Par contre, les cellules de la crête neurale doivent se déplacer pour se répartir dans le corps tout entier, pour donner des nerfs et d'autres structures. Le mouvement des cellules de la crête neurale sont indiqués dans le schéma ci-contre. On voit qu'il y a deux chemins de migration : un premier juste passe en dessous de l’ectoderme, et un autre qui s'enfonce et contourne les somites. Le premier chemin est que prennent les cellules qui donneront les mélanocytes et le squelette. Le chemin profond, quant à lui, est celui qui donne naissance au système nerveux périphérique et à la glande surrénale (sa médulla pour être précis).
Précisons que le système nerveux périphérique du visage ne provient pas de la crête neurale, mais d'autres structures anatomiques de l’ectoderme. Outre la crête neurale, une partie du système nerveux périphérique provient de placodes, des zones de l'ectoderme qui sont plus épaisses que la normale. Rappelons que l'ectoderme des placodes n'appartient pas à la plaque neurale. À vrai dire, on pourrait considérer que la plaque neurale n'est qu'une placode de grande taille, destinée à donner naissance au système nerveux central et au reste du système nerveux périphérique. Le rôle des placodes est de former les organes des sens et le tissu nerveux associé. Elles sont notamment à l'origine de l’oreille interne, du nez, du cristallin de l’œil, des papilles gustatives, et quelques autres structures sensorielles. Elles sont aussi à l'origine de certains nerfs crâniens, dont le nerf olfactif et le nerf cochléovestibulaire, le nerf facial, le nerf glosso-pharyngien et le nerf vague.
- Un chapitre entier sera dédié à la migration des neurones.
La ségrégation dorso-ventrale
[modifier | modifier le wikicode]Si on regarde le tube neural en coupe-section, on voit qu'il se subdivise en plusieurs sections : une section dorsale et une section ventrale, avec une section intermédiaire plus limitée. Les neurones de la section ventrale évoluent en motoneurones, ce qui fait que cette section devient un centre purement moteur. Par contre, la section dorsale voit ses neurones évoluer en neurones sensoriels, rendant cette section purement sensitive. Entre les deux, on trouve une fine zone intermédiaire chargé des sensations et de la motricité viscérale (interne), qui se divise en deux couches respectivement motrices et sensorielles. Cette organisation sera conservée dans la moelle épinière (dans sa substance grise, plus précisément), comme nous le verrons dans quelques chapitres. Cependant, cette subdivision ne résistera pas dans le cerveau, quoiqu'on en retrouve quelques traces dans le tronc cérébral. La partie dorsale est aussi appelée le toit, alors que la partie ventrale est appelée le plancher.
L'origine de cette subdivision est encore une fois la production de facteurs de différentiation : les BMPs et la protéine SHH. Les BMPs sont produites au sommet du tube neural et induisent la formation de neurones sensoriels, alors que la molécule SHH est impliquée dans la différentiation de la portion ventrale. On détaillera plus en détail l'action de la protéine SHH (Sonic Hedgehog) sur la portion ventrale dans le prochain paragraphe. BMPs et SHH sont produites dans deux structures anatomiques placées respectivement au sommet et au bas du tube neural. Ces deux zones portent les doux noms de plaque alaire (au sommet du tube neural) et plaque basale (en bas).
 |
 |
Après sa division en portion ventrale et dorsale, le tube neural se ségrège en plusieurs couches. La portion dorsale se subdivise en 6 couches, toutes composées de neurones sensoriels. La subdivision est induite par les protéines BMPs, comme nous l'avons dit plus haut. Ces protéines sont produites au niveau d'un groupe de cellules, qui surmonte le tube neural : la roof plate, ou plaque alaire. Les protéines BMPs se dispersent dans le tube neural, à partir de la plaque alaire, ce qui donne un gradient de concentration de BMPs. Les BMPs agissent sur la portion dorsale, mais elles n'arrivent pas jusqu'à la portion ventrale, sur laquelle elles ne peuvent pas agir. Leur action active les gènes PAX-3 et PAX-6, PAX-7 et HOX 7 (msx1), qui induisent la création de neurones dorsaux. Les cellules de la plaque neurale, dont les gènes pré-cités s'activent, se métamorphosent en neurones sensoriels dorsaux.
La portion ventrale se subdivise rapidement en 5 couches nommées V0, V1, V2, V3 et MN (MotorNeuron progenitor). Les couches V0 à V3 contiennent des interneurones, alors que la couche MN contient de futurs motoneurones (d'où son nom). À la base de la portion ventrale, on trouve aussi une plaque basale, aussi appelée floor plate. Cette subdivision est induite par diverses molécules, qui sont évidemment des facteurs de différentiation. La protéine Sonic Hedgehog, abréviée SHH, est nommée d'après la mascotte des jeux vidéos Sonic... Elle est produite par la notochorde, située sous le tube neural. La protéine se disperse depuis la notochorde et se répand dans le tube neural. Plus une cellule est proche de la notochorde, plus elle reçoit de protéine SHH. Il existe un gradient de concentration de SHH à travers le tube neural, qui induit la différentiation en couches V0-V3 et MN.
 |
 |
Suivant le seuil exact de SHH local, les neurones vont réagir différemment et se spécialiser dans de types de motoneurones différents. Si la concentration est dans tel seuil, ils vont se spécialiser dans tel type de motoneurone. Les mécanismes de ce phénomène sont assez simples. La SHH agit sur des récepteurs membranaires sur la paroi des neurones. Suivant la quantité de SHH, les récepteurs vont être plus ou moins activés et la réponse du neurone sera différente. Dans les grandes lignes, chaque intervalle de concentration en SHH active ou désactive certains gènes. Par exemple, le gène Nkx2.2 s'active au-delà d'un certain seuil, tandis que le gène Pax6 se désactive. De même, le gène Mkx6.1 s'active de même pour un autre seuil de SHH, alors que le gène Ddx se désactive pour ce même seuil. Des protéines spécifiques vont être produites suivant la concentration en SHH, et ce sont ces protéines qui vont induire la spécialisation du neurone. Parmi ces molécules, on peut citer les molécules Irx3, Olig2 et Nkx2.2.


L'implication de la notochorde a été prouvée formellement par diverses expériences. Les plus spectaculaires sont les expériences de greffe de notochorde. Elles consistent à greffer une seconde notochorde à un embryon animal, et à regarder ce qui se passe. Peu après la greffe, une seconde portion ventrale apparaît juste à côté de la notochorde greffée. On observe l'apparition d'une floor plate, ainsi qu'une différentiation des neurones en motoneurones, l'apparition de plusieurs couches de neurones, bref : une portion ventrale indiscernable d'une portion ventrale normale.
La régionalisation antéro-postérieure
[modifier | modifier le wikicode]Par la suite, le tube neural va se différencier entre cerveau et moelle épinière, puis se segmenter en morceaux de plus en plus petits. Chaque morceau donnera naissance à une aire cérébrale bien précise, ou au moins à une structure anatomique distincte des autres. Le morcellement du tube neural sur l'axe pied-tête, aussi appelé processus de régionalisation antérieur-postérieur ou différenciation antérieur-postérieur, est encore mal compris chez les vertébrés. Fait important, ce processus commence dès l'étape de neurulation, dans la plaque neurale, mais il se poursuit bien après.
La régionalisation antérieure-postérieure est le résultat de l'expression de divers gènes, dont les fameux gènes Hox (les homéogènes, impliqués dans la morphologie générale des animaux) sont les plus connus. L'expression de ces gènes suit souvent un gradient sur l'axe antérieur-postérieur : certains s'exprimant sur toute la longueur du tube neural, d'autres seulement sur la portion antérieure, d'autres sur la portion postérieure, d'autres entre les deux, d'autres sur seulement une zone très précise, etc. Ces gènes produisent des facteurs de différenciation qui favorisent la subdivision du tube neural. Beaucoup de candidats sont en lice, mais les chercheurs ont peu de certitudes à l'heure actuelle. Suivant les gènes exprimés à un endroit, et donc les protéines produites, les cellules vont se spécialiser en neurones spécialisés (en neurones dopaminergiques, en cellules pyramidales, ...).
L'exemple le plus important est de loin celui des gènes Hox, aussi appelés homéogènes. Ce sont des gènes impliqués dans la morphologie générale des animaux, dans le plan d'organisation anatomique, bien que leur fonction varie beaucoup suivant l'espèce animale considérée. Chez la mouche drosophile, les homéogènes organisent l'axe antérieur-postérieur de l'animal en plusieurs segments distincts, et le transforment pour donner des ailes, antennes, ou autres. Pour être plus clairs, ils imposent la position des ailes, des antennes, ou d'autres structures anatomiques. Chez les vertébrés, ils ont un rôle similaire, mais nous allons nous concentrer sur leur rôle dans l'organisation du tube neural. Les homéogènes segmentent le tube neural en plusieurs sections, en segments, dont l'utilité est déterminée par leur position : tel segment va donner la moelle épinière sacrée, tel autre la moelle épinière thoracique, tel autre le cervelet, tel autre telle aire cérébrale, etc. Chez l'homme (et les vertébrés en général), le grand nombre de protéines Hox permet de segmenter le tube neural en un grand nombre de segments divers, permettant une spécialisation accrue du système nerveux. La segmentation induite par les gènes Hox est illustrée dans le schéma ci-dessous, pour plusieurs espèces animales.

La séparation du cerveau de la moelle épinière
[modifier | modifier le wikicode]Une première segmentation sépare le cerveau de la moelle épinière. Certains facteurs de différentiation sont produits au niveau de la tête et induisent la formation du cerveau, tandis que d'autres sont produit dans le reste du tube neural, induisant la formation de la moelle épinière. La plaque neurale produit de nombreux facteurs de différentiation : des WNTs (wingless related), des FGFs (fibroblast growth factors), des RA (acides rétinoïques), et d'autres protéines. Le tissu nerveux se différencie en moelle épinière, sous l'influence de ces WNTs, FGFs, RA (acide rétinoïque), et autres. Mais au niveau de la tête, ce processus est supprimé par l'action d'inhibiteurs qui coupent l'action de ces facteurs de différentiation.
Un exemple frappant est la répartition de l'acide rétinoïque dans le cerveau en développement. L'acide rétinoïque est produit essentiellement dans les régions postérieures, au niveau de la moelle épinière et du myélencéphale. L'acide rétinoïque se disperse ensuite dans le reste du cerveau, ce qui forme un gradient de concentration en acide rétinoïque. Mais dans les régions antérieures, diverses enzymes dégradent l'acide rétinoïque, la principale étant la CYP26. L'acide rétinoïque ne peut pas faire son effet, et on obtient bien une distinction entre région antérieure et postérieure.
La segmentation du cerveau
[modifier | modifier le wikicode]
Le processus de segmentation se poursuit ensuite dans le cerveau et la moelle épinière. Au niveau du cerveau, la partie la plus proche de la future tête grossit progressivement. Elle forme trois vésicules, qui se séparent elles-mêmes en cinq structures, le tout étant illustré dans le schéma ci-contre. La formation de ces vésicules est appelée la régionalisation cérébrale. Ces cinq structures restent en place durant toute la vie du cerveau. C'est la raison pour laquelle l'anatomie du cerveau, que nous aborderons plus loin, est essentiellement structurée autour de ces cinq subdivisions.

À quatre semaines de gestation, le cerveau est subdivisé en trois vésicules : le prosencéphale, le mésencéphale et le rhombencéphale. Le tube neural a alors une forme légèrement courbée, sans replis majeurs. Les trois vésicules primordiales sont déjà visibles avant la formation du tube neural. Dès la formation de la plaque neurale, on observe des indentations et des renflements latéraux qui préfigurent les trois vésicules primordiales. On les voit dès le 19ème jour de gestation, soit avant le début de la courbure de la plaque neurale.
Entre la quatrième et la huitième semaine de gestation, le tube neural se replie et forme trois coudes assez importants. Ils se situent entre le cerveau et la moelle épinière, au niveau du mésencéphale et au niveau du pont cérébral. Le repli au niveau du mésencéphale est appelé la courbure mésencéphalique, le repli cerveau-moelle est appelé la courbure cervicale et celui au niveau du pont est appelé la courbure pontique. C'est au niveau de la courbure pontique que le quatrième ventricule s'installe.
Par la suite, le prosencéphale se subdivise en télencéphale et diencéphale, alors que le rhombencéphale se divise en myélencéphale et métencéphale. Le cerveau est alors composé de 5 vésicules distinctes. Ces divisions sont causées par l'apparition de courbures au beau milieu du prosencéphale et du rhombencéphale.
 |
 |
Au niveau du cerveau, les molécules produites dans ce processus sont illustrées ci-dessous. Le deux plus importantes sont les molécules Otx2 et Gbx2. Otx2 est exprimée dans les portions antérieures du cerveau, et induit la formation du prosencéphale et du mésencéphale. Au contraire, Bgx2 est produit dans la portion postérieure et induit la formation du métencéphale et du myélencéphale. À la limite entre les deux, Otx2 et Gbx2 ne s'expriment pas ou trop peu, ce qui donne naissance à l'organisateur isthmique, la frontière entre mésencéphale et métencéphale. Cette région est destinée à former le cervelet et quelques autres aires cérébrales. Une fois formé, l'organisateur isthmique produit de nombreuses molécules impliquées dans le développement : la FGF8, la Wnt1, la En1, etc. Sans cet isthme et les cellules qu'il contient, la régionalisation ne se passe pas correctement. Si on retire l'organisateur isthmique, les structures du cervelet et du tectum ne se forment pas du tout.

Outre l'organisateur isthmique, d'autres structures embryonnaires influencent la spécialisation des aires cérébrales. Au niveau du prosencéphale, il n'y a pas de notochorde, ce qui fait que les processus de différentiation sont assez spécifiques. Il existe cependant une plaque pré-chordale en dessous du tube neurale, qui produit des facteurs de différentiation tels que Emx (Empty spiracle), Lim et Otx (Orthodenticle). Ils favorisent la formation de tissus typiques du télencéphale et du diencéphale. Au niveau du mésencéphale et du rhombencéphale, l'organisateur isthmique joue son rôle et produit des facteurs de différentiation. Cependant, la notochorde va aussi produire des facteurs de différentiation qui vont agir sur le rhombencéphale, mais pas sur le mésencéphale. Les deux structures vont donc évoluer de manière différente. Enfin, au niveau de la moelle épinière, on observe l'influence à la fois de la notochorde, mais aussi de l'acide rétinoïque.

Une fois la régionalisation terminée, le tube neural se subdivise en plusieurs segments, appelés des neuromères. En tout, on peut compter 1 neuromère télencéphalique, 4 neuromères diencéphaliques, 2 neuromères mésencéphaliques (C), et 8 neuromères rhombrencéphaliques (D). Les neuromères du rhombrocéphale sont appelés des rhombromères, ils sont au nombre de 8 et sont notés R1, R2, R3, R4, R5, R6, R7, R8. La subdivision en rhombromères ne survit pas, les neurones finissant par migrer progressivement dans leur position finale. Elle est certainement utile pour induire la fonction des neurones, ce à quoi ils vont servir, quitte à devoir les déplacer vers les noyaux finaux si besoin. Au passage, précisons que chaque rhombromère donne naissance à un ensemble bien précis de nerfs crâniens. Au passage, les rhombromères donnent aussi naissance au cervelet.
Les cellules des rhombromères se reproduisent et se divisent, la neurogenèse étant assez importante, mais elles ne peuvent pas franchir les limites des rhombromères. On se demande encore comment les neurones connaissent les limites des rhombromères et ce qui les empêche de franchir la limite. On suppose que les neurones de rhombromères pairs ne peuvent pas se coller aux cellules des rhombromères impairs, parce qu'ils expriment des protéines d'adhésion cellulaire différentes. Diverses expériences ont montré que les neurones des rhobromères pairs peuvent se mélanger entre eux, idem pour les neurones des rhombromères impairs, mais que les impairs ne peuvent pas se mêler aux pairs et réciproquement. La subdivision en rhombromères est probablement induite par l'expression des gènes Hox, qui est différente dans chaque rhombromère : le segment R1 n'exprime aucun gène Hox, le R2 exprime le gène HoxA2, le R3 exprime le HoxB2, le R4 exprime les gènes HoxA1 et HoxB1, etc. Les gènes Hox fournissent donc une information sur la position spatiale de chaque rhombromère, information qui indique aux neurones comment ils doivent évoluer.
La segmentation de la moelle épinière
[modifier | modifier le wikicode]La segmentation de la moelle épinière donne naissance aux différents segments médullaires (les segments de la moelle épinière, chacun associé à une vertèbre/un dermatome). Comme pour les rhombromères, chaque segment est associé à des nerfs périphériques distincts. On rappelle que chaque segment médullaire donne naissance à une paire de nerf spinaux qui sort de la moelle épinière pour innerver le reste du corps. Le processus de segmentation est assez similaire à la formation des rhombromères cérébraux. Mais le processus de segmentation se fait en plusieurs étapes, et non en une seule fois.
La première étape est la séparation en trois régions : une région cervicale, une région thoracique et une région lombaire-sacrée. Cette subdivision est induite par une protéine : la FGF, qui active ou désactive les gènes HoxC6 et HoxC9 selon sa concentration. Elle est produite dans la région postérieure, ce qui crée un gradient de concentration sur l'axe antérieur-postérieur. Ce gradient active le gène HoxC9 dans la région postérieure et active le gène HoxC6 dans la région antérieure.

Le développement du cerveau
[modifier | modifier le wikicode]
Une fois l'étape de régionalisation terminée, le cerveau va continuer à se développer et divers processus vont modifier la forme du cerveau, la position des neurones, et la quantité de synapses. Dans les grandes lignes, la régionalisation cérébrale se combine avec la ségrégation dorso-ventrale. Les vésicules conservent une séparation entre toit et plancher (aussi appelés plaque alaire et plaque basale). Les futures aires cérébrales vont se former soit dans le toit, soit dans le plancher, très rarement dans les deux. Par exemple, le cervelet se forme dans le toit du métencéphale, le plancher donnant grossièrement le pont de Varole. Mais la formation des aires cérébrales ne se fera pas exactement de la même manière dans le cortex cérébral et dans le reste du cerveau. La mise en place du cortex est le fait de processus assez spécialisés, qui ne sont pas les mêmes que ceux qui donnent les noyaux cérébraux.
Le développement du tronc cérébral
[modifier | modifier le wikicode]Le tronc cérébral est essentiellement composé de noyaux cérébraux, sans la moindre présence de cortex. La formation des noyaux est une simple poursuite des processus de segmentations vus précédemment. La substance grise se subdivise de plus en plus finement, pour donner les noyaux cérébraux. À la nuance près que les neurones des noyaux se forment dans la couche ventriculaire et qu'il y a des processus de migration qui déplacent les neurones vers leur position finale.
Les colonnes neurales du tronc cérébral
[modifier | modifier le wikicode]Dans les grandes lignes, le tube neural se subdivise en plusieurs colonnes verticales, qui courent sur la longueur du futur tronc cérébral. Ces colonnes se coupent ensuite sur leur longueur et forment plusieurs noyaux, dont les noyaux des nerfs crâniens. Il y a en tout 7 colonnes distinctes, regroupées en 4 colonnes sensorielles et 3 colonnes motrices, et 4 colonnes somatiques et 3 viscérales.
Les colonnes alaires naissent au niveau du toit du tube neurale, de la plaque alaire (d'où leur nom). Elles donnent naissance à des noyaux sensoriels, en accord avec la spécialisation sensorielle de la portion dorsale du tube neurale. Deux de ces colonnes donnent des noyaux dédiés à la sensibilité somatique, consciente. Elles sont naturellement appelées colonnes afférentes somatiques. À l'opposé, les deux autres colonnes donnent des noyaux viscéraux, à savoir spécialisés dans la sensibilité inconsciente. Elles sont appelées colonnes afférentes viscérales. Les quatre colonnes sont les suivantes :
- La colonne afférente viscérale générale donne naissance à une partie du noyau du tractus solitaire, un noyau impliqué dans la sensibilité viscérale du tube digestif.
- La colonne afférente viscérale spéciale donne naissance aux nerfs crâniens VII, IX et X et à une partie du noyau du tractus solitaire.
- La colonne afférente somatique générale donne naissance aux noyaux des nerfs crâniens V, VII, IX et X.
- La colonne afférente somatique spéciale donne naissance au noyau du nerf crânien VIII.
Les colonnes ventrales, aussi appelée colonnes fondamentales sont à l'origine des noyaux moteurs. Elles naissent dans la portion ventrale du tube neurale. En conséquence, elles donnent des noyaux moteurs. Deux de ces colonnes donnent des noyaux spécialisés dans la motricité involontaire, aussi appelée motricité viscérale. Elles sont appelées colonnes efférentes viscérales. La colonne restante, la colonne efférente somatique générale donnent des noyaux moteurs qui prennent en charge la motricité volontaire, consciente. Pour résumer, voici les trois colonnes fondamentales :
- La colonne efférente somatique générale donne naissance aux noyaux des nerfs crânien XII (nerf hypoglosse), III, IV, et V (oculomoteurs).
- La colonne efférente viscérale spéciale donne naissance aux noyaux des nerfs crâniens V, VII, IX, X, XI.
- La colonne efférente viscérale générale donne naissance aux noyaux du nerf vague (pneumogastrique), des noyaux salivaires supérieur et inférieur, du nerf facial, du nerf glosso-pharyngien et du nerf oculomoteur III (Edinger-Westphal).
Le développement régional du tronc cérébral
[modifier | modifier le wikicode]Une fois les colonnes formées, elles se subdivisent en noyaux indépendants. De plus, certaines portions de la substance grise vont s'individualiser pour donner des structures spécialisées. Pour rentrer plus dans le détail, il faut regarder ce qu'il se passe dans chaque structure, comment elle se subdivise. Dans ce qui va suivre, nous allons partir des zones proches de la moelle, avant de progresser vers le télencéphale.
Commençons donc par le myélencéphale caudal, la portion du myélencéphale la plus proche de la moelle épinière. À ce niveau, le toit du tube neural donne naissance aux noyaux gracile et cunéiforme, deux noyaux de la sensibilité corporelle. Ils se forment par migration des neurones dans la couche marginale, la substance grise se déformant et faisant saillie dans la substance blanche. Progressivement, la saillie prend une forme sphérique et se coupe de la substance grise. Dans la partie ventrale, la substance grise reste en place et la substance blanche se développe en priorité. Vers le quatrième mois, le faisceau pyramidal traverse cette section.
La partie rostrale du myélencéphale, celle située au bord du métencéphale, se développe différemment. La raison à cela est que le quatrième ventricule se met en place à cet endroit. La lumière du tube neural gonfle pour donner le ventricule, ce qui compresse le tube neural sur ses parois externes. Le tube neural est repoussé sous les futurs ventricules, au point que le toit et le plancher se retrouvent tous deux sous le ventricule. Là, toit et plancher se subdivisent en colonnes verticales, qui se subdivisent ensuite en divers noyaux cérébraux. La plupart des noyaux proviennent du plancher, à l'exception des noyaux de l'olive bulbaire, dont les neurones naissent dans le toit mais migrent dans la partie ventrale. Au-dessus des ventricules, au niveau du toit, la substance grise et la substance blanche ont été complètement repoussés et il ne reste qu'une simple toile très fine composée uniquement d'épendymocytes. Cette toile est appelée la toile choroïdienne du 4e ventricule, et évolue en plexus choroïdes.

|

|
| Tube neural dans le myélencéphale rostral, après 38 jours de gestation. | Tube neural dans le myélencéphale rostral, après 44 jours de gestation. |

Au niveau du métencéphale (le pont de Varole), le développement est identique à celui du myélencéphale rostral, en raison de la présence du quatrième ventricule. La plaque alaire est repoussée en dessous du futur ventricule, de même que le plancher. Cependant, elle va proliférer et donner naissance à de nouveaux neurones, qui vont migrer en position dorsale. Ils vont remonter au-dessus du ventricule et former une sorte d'excroissance sur les bords de l'ancien toit. Le résultat est que le tube neural ne semble pas tout à fait fermé, mais semble entrouvert. Vu de l'extérieur, le tube neural a une forme de bouche, avec deux lèvres distinctes et séparées. Cette structure anatomique porte le nom de lèvres rhombiques. Par la suite, les lèvres rhombiques vont se rapprocher au point de se fermer. Le résultat de cette fermeture est un renflement perpendiculaire au tronc cérébral : la plaque cérébelleuse. Elle est appelée ainsi car c'est elle qui va évoluer pour donner le cervelet. Vers la 12e semaine, la plaque cérébelleuse s'épaissit et diverses fissures apparaissent. Ces fissures sont équivalentes aux sillons qui séparent les lobes du cortex. Elles vont séparer le cortex du cervelet en plusieurs lobes, aux fonctions distinctes. Puis, le cortex cérébelleux va se replier sur lui-même, comme le cortex cérébral, et donner des sillons et gyri.
Pour le mésencéphale, le toit et le plancher auront des destinées différentes, de même que la substance blanche. Rappelons que le mésencéphale est composé de trois structures, quand on le regarde en section. Une région ventrale est juxtaposée au tegmentum, accolé lui-même au tectum. Le tectum est composé de quelques noyaxu, de même que le tegmentum. Par contre, la région ventrale est surtout composée de fibres de substance blanche. La région ventrale est ce qu'il reste de la couche marginale, la couche de substance blanche du tube neural. Le tegmentum et le tectum proviennent de la substance grise : le toit donne le tectum, alors que le plancher donne le tegmentum.
Le développement du diencéphale
[modifier | modifier le wikicode]Le diencéphale et le télencéphale naissent à partir du prosencéphale. La subdivision entre les deux commence à la 5e semaine, quand deux vésicules télencéphaliques se forment. Elles grossissent alors et gonflent massivement, au point de recouvrir le diencéphale. Le diencéphale, lui, garde plus ou moins sa forme initiale : il ne grossit pas beaucoup. L'évolution du tube neural dans le diencéphale se caractérise par une forte réduction du plancher, alors que le toit prend de plus en plus de place. En conséquence, on ne trouve pas beaucoup de structures purement motrices (donc ventrales) dans le diencéphale, alors que les structures sensorielles sont plus nombreuses. Cela explique aussi le développement du thalamus, et des structures annexes, qui proviennent du toit.
Le diencéphale est situé non loin du troisième ventricule, ce qui fait que son évolution ressemble beaucoup à celle du myélencéphale rostral. Le troisième ventricule repousse la substance grise au-dessous de lui, et il ne reste à son sommet qu'une fine couche d'épendymocytes. Cette couche donne naissance aux parois ventriculaires et aux plexus choroïdes, mais aussi les organes circumventriculaires, des aires cérébrales qui ne sont pas protégées par la barrière hémato-encéphalique.
Le toit, la plaque alaire, donne naissance à diverses structures anatomiques, dont les principales sont la glande pinéale, au thalamus, et à l'hypothalamus. À la 7e semaine, des excroissances se forment, s'invaginent et pénètrent dans le ventricule. Une de ces excroissances, appelée l'éminence ganglionnaire, un lieu de fabrication de nouveaux neurones. Elle se forme au niveau de la plaque alaire (le "toit"), quand des neuroblastes migrent dans la substance blanche de la couche marginale. Les neurones fabriqués dans cette zone migrent ensuite dans le cortex et le reste du télencéphale.
La séparation entre thalamus et hypothalamus se fait assez précocement. Elle est le fait de l'apparition du sillon longitudinal sous-thalamique. Ce sillon est entouré par deux renflements, appelés renflement thalamique et renflement hypothalamique. Ils donnent respectivement naissance au thalamus et à l'hypothalamus. Un autre renflement, localisé ailleurs, donnera naissance à la glande pinéale.
L'hypophyse a une formation qui est un peu à part. Dans les grandes lignes, elle se forme à partir de deux sources : une partie provient du tissu nerveux du tube neural, une autre est un tissu endocrine qui se forme à partir de l'ectoderme. La partie glandulaire se forme juste au-dessus de la notochorde, dans l'ectoderme local. Une partie de l'ectoderme se replie et s'invagine, formant la poche de Rathke. Elle se détache ensuite et part à la rencontre de la portion nerveuse de l'hypophyse. De l'autre côté, la portion nerveuse se forme de la même manière, par invagination de la paroi du tube neural. Mais elle ne se détache pas et reste en contact avec elle. L'invagination neurale prend une forme de poche gonflée, reliée au reste du tube neural par une tige. La poche de Rathke et l'invagination neurale se rencontrent et se juxtaposent l'une contre l'autre, formant l'hypophyse proprement dite.
Le développement du cortex
[modifier | modifier le wikicode]Dans le telencéphale, le toit et le plancher donnent des structures différentes : cortex pour le toit, ganglions de la base pour le plancher. Le cortex se met en place suite à l'intervention de divers processus, qui portent les noms de neurogenèse, de migration et de gyration. Ils sont décrits succinctement dans le tableau ci-dessous.
| Étape | Description | Temps écoulé depuis la conception |
|---|---|---|
| Neurogenèse | Fabrication de nouveaux neurones. | Majoritairement entre la 7e et la 16e semaine, plus rare ensuite. |
| Migration | Déplacement des neurones dans leur position définitive, formation des couches du cortex. | Entre le 3e et le 6e mois. |
| Gyration | Formation des gyrus et sillons à la surface du cortex. | Entre la 22e semaine et l'âge de 2 ans. |
La production de cellules neurales est généralement très intense lors du développement, avec un pic de 250 000 neurones crée par secondes au paroxysme. Mais cela ne dura qu'un temps, la production de neurones finissant par s'arrêter dans la quasi-totalité du cerveau. Après la régionalisation, les cellules souches seront toutes devenues des neurones ou des cellules gliales. C'est ainsi : les neurones d'un adulte ne se régénèrent pas, sauf dans quelques régions cérébrales qui font exception à la règle. Les zones du cerveau où la neurogenèse continue à l'âge adulte sont limitées à l'hippocampe et au bulbe olfactif, deux zones du cerveau que nous verrons dans quelques chapitres.
Une fois les neurones et cellules gliales formés, ils vont se déplacer jusqu’à leur position finale dans le système nerveux. L'ensemble de ce processus de déplacement est appelé la migration. Dans le système nerveux central, les neurones naissent sur la paroi des ventricules. Ils vont ensuite se déplacer jusqu'à leur destination. Lors de ce processus, les premiers neurones vont donc former une première couche de neurones, qui sera surmontée par une couche de neurones produits ultérieurement. Cette seconde couche sera ensuite recouverte par une couche produite encore après elle, et ainsi de suite. Cela peut paraître bizarre, surtout que les neurones sont produits en dessous des couches déjà formées, mais c'est pourtant la réalité. Les neurones produits en dernier vont traverser les couches déjà construites. Le résultat de cette migration est une structuration en couches de neurones, qui donne naissance au cortex cérébral. Le résultat est une organisation en 6 couches pour le néocortex, 3 à 4 pour les paléo et archi-cortex.
Le cerveau d'un fœtus est ainsi plat dans les premières semaines après sa formation. Mais par la suite, le cortex se replie sur lui-même, ce qui donne naissance aux premiers sillons et gyrus. Les gyrus s'installent alors progressivement avec l'augmentation de la taille du cerveau. Ce développement des circonvolutions est appelé la gyration.


Après l'étape de migration/gyration, les neurones sont à leur position définitive. Les synapses peuvent alors se former. Chaque neurone va former un ou plusieurs axones, qui s'étendront progressivement. Chaque axone se déplacera et sera guidé vers sa cible finale par divers gradients chimiques. Le processus final donne naissance à un grand nombre de synapses, le nombre maximal de synapses étant atteint vers 2 ans. Mais beaucoup de ces synapses sont des synapses « inutiles ». Divers processus liés à la plasticité synaptique vont alors sélectionner les synapses les plus « utiles », les autres périclitant. Ainsi, le nombre de synapse diminue rapidement après 2 ans, avant de se stabiliser. Mais la formation de nouvelles synapses est toujours possible, à tout âge, sous certaines conditions.
Mais outre l'augmentation du nombre de synapses, l'efficacité des synapses existantes va aussi augmenter. Les axones vont progressivement se recouvrir d'une gaine de myéline, fabriquée par les oligodendrocytes. Ce processus de myélinisation se poursuit durant l'enfance et l'adolescence. Il commence d'abord par se faire sentir dans les zones situées à l'arrière du cerveau, pour finir sur les zones situées sous le front. On estime que ce processus se poursuit jusqu'à la fin de l'adolescence, voire jusqu'au début de l'âge adulte.
En savoir plus
[modifier | modifier le wikicode]Pour ceux qui veulent en savoir plus, ou qui veulent une présentation différente ce celle du chapitre, je conseille la lecture du site web suivant :
Si vous voulez en savoir sur le développement de l'embryon en général, vous pouvez lire le site web complet, et pas seulement la section sur le système nerveux. Voici le lien pour le site web complet :

