Pathologie/Pathologie générale/Inflammation aiguë
INFLAMMATION AIGUË
Causes
[modifier | modifier le wikicode]- Brûlure
- Engelure
- Infections
- Dépôts de substance anormales
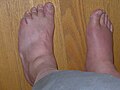
- Dépôt d'urates : La goutte
Phases de l'inflammation aiguë
[modifier | modifier le wikicode]Phase vasculaire de l'inflammation
[modifier | modifier le wikicode]Les réactions vasculo-sanguines regroupent 3 phénomènes : - la congestion active - l’œdème inflammatoire - la diapédèse leucocytaire
Vasodilatation et congestion
[modifier | modifier le wikicode]La congestion (du latin congestio, amas, de congerere, accumuler) est l'augmentation subite de la quantité de sang contenue dans les vaisseaux sanguins d'un organe ou d'une partie d'organe, comme un tissu biologique.
Elle est en général associée à une dilatation des vaisseaux sanguins, ou vasodilatation.
La congestion active est due à une vasodilatation survenant après une brève phase de vasoconstriction qui favorise l'hémostase. Elle est artériolaire puis capillaire, d'où une augmentation du débit sanguin mais un ralentissement circulatoire. Elle se traduit par une distension des capillaires qui apparaissent gorgés de sang, bordés par un endothélium turgescent. Elle est à l'origine de la rougeur cutanée de l'inflammation comme après un coup de soleil.
Elle est déterminée par: - un mécanisme nerveux (nerfs vasomoteurs) - un mécanisme chimique impliquant l'histamine, la sérotonine, les kinines et les prostaglandines et les leucotriènes. L'action de l'histamine mastocytaire n'explique que les réactions vasculaires précoces, qui sont relayées notamment par les kinines.
Œdème
[modifier | modifier le wikicode]L’œdème inflammatoire est un phénomène actif dû au passage, à partir des vaisseaux congestifs, vers le milieu interstitiel, espace virtuel pouvant se remplir d'un liquide proche du plasma. Ce passage est lié à l'augmentation de la pression hydrostatique et surtout à l'augmentation de la perméabilité de la paroi vasculaire des capillaires et des veinules.
L’œdème a pour conséquence: - de diluer le foyer inflammatoire - de limiter ce foyer par une barrière fibrineuse (fibrinogène) - de concentrer sur place les moyens de défense humoraux (immunoglobulines, complément) et apporter des médiateurs chimiques - de ralentir le courant circulatoire par hémoconcentration, ce qui favorise le phénomène suivant, la diapédèse leucocytaire.
L’œdème inflammatoire donne dans une cavité un exsudat riche en protéines, ce qui l'oppose au transsudat.
Prédominance de la réaction vasculaire
[modifier | modifier le wikicode]La prédominance de la réaction vasculaire caractérise les inflammations aiguës. Elles ont généralement un début brutal et une évolution brève.
On en distingue cinq formes:
- L'inflammation congestive: elle est fugace, rapidement résolutive, traduite par une simple congestion artériolaire et capillaire. exemple: l'érythème solaire
- L'inflammation œdémateuse: elle est caractérisée par une exsudation séreuse pauvre en fibrine. exemples: l'urticaire, l'œdème de Quincke
- L'inflammation fibrineuse: elle comprend une exsudation plasmatique plus ou moins riche en fibrine, qui peut aboutir par coagulation de la fibrine à la constitution de dépôts solides. exemples: les fausses membranes de l'angine diphtérique; enduit fibrinoleucocytaire de l'ulcère gastrique
- L'inflammation fibrino-leucocytaire: associé à un exsudat fibrineux, l'afflux leucocytaire est plus ou moins important, par diapédèse. exemple: l'alvéolite fibrino-leucocytaire de la pneumonie
- L'inflammation hémorragique: il existe une infiltration d'hématies extravasées. Cette érythrodiapédèse est la conséquence d'une fragilisation de l'endothélium. Elle est due à l'agent pathogène lui-même ou à une perturbation vasculaire antérieure avec stase. exemple: le syndrome grave des maladies infectieuses, les fièvres hémorragiques d’origine virale
Exemples
[modifier | modifier le wikicode]- Infections à pyogènes
- La goutte
-
The gout james gillray
-
Gout Signs and Symptoms
-
Gout Advanced
-
En.Wikipedia-VideoWiki-Gout
-
Gout 01a
Phase cellulaire de l'inflammation
[modifier | modifier le wikicode]L'érythrodiapédèse est un phénomène pathologique traduit par le passage d'hématies hors des vaisseaux, ce qui détermine des hémorragies interstitielles. Elle implique des lésions des parois capillaires; elle est importante dans certaines inflammations.
La diapédèse leucocytaire est la traversée active des parois vasculaires par les leucocytes. Elle a surtout été étudiée sur les polynucléaires mais intéresse également les lymphocytes et les monocytes circulants. Elle est favorisée par le ralentissement circulatoire, la turgescence endothéliale, l'afflux leucocytaire. Elle débute par la margination des leucocytes qui adhèrent à la paroi endothéliale. Les polynucléaires émettent ensuite des pseudopodes, s'infiltrent entre les cellules endothéliales, puis traversent la membrane basale. L'accolement se fait grâce à l'interaction des molécules d'adhérence spécifiques présentes à la surface de la cellule endothéliale et du polynucléaire. Morphologiquement, la diapédèse leucocytaire se manifeste par un infiltrat inflammatoire périvasculaire.
Physiopathogénie
[modifier | modifier le wikicode]Les phénomènes vasculo-exsudatifs initiaux permettent l'arrivée dans le foyer inflammatoire des leucocytes. Les premiers sur place (environ 6 heures) sont les polynucléaires. Ils sont le stigmate morphologique d'une inflammation aiguë. En fonction de la cause de l'inflammation, ceux-ci pourront persister sur place et s'accumuler en étant à l'origine d'une suppuration. Le plus souvent, les polynucléaires sont progressivement remplacés sur le site inflammatoire par les cellules mononucléées. Parmi celles-ci, les macrophages ont pour fonction d'assurer la détersion grâce à leur capacité de phagocytose. Il s'y associe des lymphocytes et des plasmocytes qui participent à la réponse immune spécifique de l'antigène. Lorsque l'inflammation persiste, l'infiltrat inflammatoire est généralement constitué d'une majorité de cellules mononucléées.
Les cellules de l'inflammation
[modifier | modifier le wikicode]Les cellules de l'inflammation comprennent 1) les lymphocytes, 2) les cellules phagocytaires ou phagocytes (polynucléaires -principalement neutrophiles- et monocytes-macrophages), 3) les mastocytes et les polynucléaires basophiles, 4) les fibroblastes.
Les cellules phagocytaires ou phagocytes comprennent les polynucléaires neutrophiles et les cellules du système monocyte-macrophage (incluant les histiocytes résidents, c'est à dire les macrophages des tissus comme les cellules alvéolaires du poumon ou les cellules de Küpffer du foie). La cellule microgliale est le macrophage du cerveau.
Polynucléaires neutrophiles
[modifier | modifier le wikicode]Macrophages et histiocytes
[modifier | modifier le wikicode]Lymphocytes
[modifier | modifier le wikicode]Les lymphocytes, cellules de l'immunité spécifique, humorale et cellulaire, sont de type B (CD20), T (CD3) ou ni B ni T (NK pour natural killer) voir polycopié d'histologie. Parmi les lymphocytes T, certains sont dits auxiliaires = « helper » (CD4), d'autres, cytotoxiques (CD8). Les lymphocytes sont la mémoire de l'immunité acquise et servent à son expression : les plasmocytes, par exemple, étape finale de la maturation de la lignée B, sécrètent les anticorps. Les lymphocytes T secrètent des cytokines. Les lymphocytes NK peuvent avoir une action cytotoxique.
Mastocytes et polynucléaires basophiles
[modifier | modifier le wikicode]Les mastocytes et les polynucléaires basophiles comportent des granulations qui contiennent des médiateurs chimiques de l'inflammation, en particulier l'histamine et l'héparine.
Les médiateurs chimiques de l'inflammation
[modifier | modifier le wikicode]Le déclenchement et la poursuite de l'inflammation, sa diffusion à partir du foyer inflammatoire initial font appel à des facteurs chimiques (radicaux libres, protéines, lipides) qui sont synthétisés localement ou qui sont à l'état de précurseur inactif dans la circulation sanguine. L'amplification local et systémique du phénomène inflammatoire est exemple typique des mécanismes de signalisation biologique, ou biosémiotique.
Facteurs d'origine locale
[modifier | modifier le wikicode]1. Amines vasoactives : Histamine et Sérotonine
Les Amines vasoactives (Histamine et Sérotonine) sont stockées dans les mastocytes, les polynucléaires basophiles, les plaquettes. Libérées dans l'espace extracellulaire, ou espace interstitiel, elles produisent une vasodilatation et une augmentation de la perméabilité vasculaire (congestion active et œdème inflammatoire).
2. Prostaglandines et leucotriènes
Les Prostaglandines et leucotriènes sont des acides gras comportant 20 atomes de carbones (= eicosanoïdes), synthétisés dans les membranes cellulaires des cellules inflammatoires à partir de l'acide arachidonique.
Produits localement, ils ont des effets locaux (vasodilatation, douleur, attraction des polynucléaires) et généraux ("systémiques"), tels que la fièvre, l'altération de l'état général, l'amaigrissement.
3. Cytokines
Les Cytokines sont des peptides ou des protéines produites par de nombreuses cellules inflammatoires, parmi lesquelles les lymphocytes (principalement des lymphocytes T CD3+) et les monocytes / macrophages ou histiocytes.
Les cytokines peuvent être considérées comme des hormones produites par des cellules isolées, plutôt que par des glandes dans le cas de la sécrétion endocrine.
Comme les hormones, elles agissent, par l'intermédiaire de récepteurs membranaires, sur la cellule qui les produit (effet autocrine), sur des cellules proches (effet paracrine), et sur des cellules situées à distance (effet endocrine).
Certaines cytokines sont pro-inflammatoires (interleukine 1 ou IL1, IL6 et tumor necrosis factor ou TNF-alpha) ; d'autres au contraire sont anti-inflammatoires (IL4, IL10, et IL13).
Les cytokines ont de nombreux effets[1]. Parmi ceux-ci, nous en retiendrons 3 principaux : a. Médiation de l'immunité naturelle : Certaines cytokines favorisent l'immunité naturelle (c'est à dire non spécifique) : c'est le cas des interférons qui provoquent l'apparition dans la cellule d'une activité antivirale non spécifique. b. Régulation de l'activation, de la croissance et de la différentiation des lymphocytes
Selon le type de l'activation lymphocytaire, l'inflammation met principalement en jeu l'immunité cellulaire ou au contraire la sécrétion d'anticorps (Immunité humorale).
La réaction cellulaire est surtout marquée lorsque l'agent infectieux est intracellulaire (virus, mycobactéries, certains parasites). La sécrétion d'anticorps, au contraire, est importante lorsque l'agression fait intervenir des pathogènes extracellulaires, bactéries ou parasites. Le type de la réaction inflammatoire est déterminé par les cytokines sécrétées par les lymphocytes T.
Celles qui favorisent l'immunité cellulaire sont dites de type Th1 (exemples qu'il est inutile de mémoriser pour ce cours : IL2, interféron gamma, IL12 et TNF-bêta) ; celles de type Th2 orientent vers la sécrétion d'anticorps (IL4, IL5, IL6, IL10, and IL13).
c. Stimulation de l'hématopoïèse
Certaines cytokines (appelées « colony stimulating factors » ou CSF) sont capables de stimuler spécifiquement la prolifération de différentes lignées hématopoïétiques (hématopoïèse), par exemple, les lignées produisant les polynucléaires, les macrophages ou les mégacaryocytes.
4. Molécules d'adhérence
Les cellules du foyer inflammatoire sont concentrées à l'endroit précis de l'organisme où l'agression a eu lieu. Ce ciblage est le résultat d'interactions complexes de molécules d'adhérence et de leurs ligands cellulaires, qui, par exemple, augmentent ou diminuent l'adhérence au tissu interstitiel. Les vaisseaux du foyer expriment des molécules d'adhérence pour retenir les cellules sanguines qui portent le ligand correspondant.
5. Médiateurs circulants (plasmatiques)
Les médiateurs circulants ne sont actifs qu'à la suite d'une cascade de réactions qui permet d'en réguler la production.
1. Le système des kinines : Les kinines proviennent du kininogène activé par la kallikréine, elle-même issue du clivage de la prékallikréine circulante. Le facteur XII (Hageman) activé est l'une des molécules qui clive la prékallikréin. Les kinines sont de puissants vasodilatateurs. Elles augmentent la perméabilité vasculaire. La bradykinine est un médiateur de la douleur.
2. Le système du complément regroupe un ensemble de protéines sériques (les facteurs du complément) dont l'activation s'effectue par des réactions de protéolyses en cascade. Les facteurs sont numérotées (C1, C3, C5 ...). Une lettre minuscule est éventuellement associée pour décrire le fragment C3a, C3b) Les fragments libérés ont des effets spécifiques, pour la plupart en rapport avec l'inflammation. Le système est activé par la réaction antigène-anticorps (c'est la « voie classique »), ou par divers composés provenant en particulier de micro-organismes comme les bactéries (c'est la « voie alterne »). Voies classique et alterne ont l'une et l'autre la propriété d'activer C3.
Nous citerons en exemple 4 facteurs qui ont une activité spécifique : a. C3a (une « anaphylatoxine ») : ce facteur provoque la dégranulation des mastocytes et des polynucléaires basophiles (dégranulation qui peut causer le choc anaphylactique). b. C3b (une « opsonine ») ce facteur adhère aux bactéries et permet leur phagocytose (« opsonification ») par des cellules phagocytaires pourvues des récepteurs correspondants. c. Le complexe C5b-9 est un « complexe d'attaque membranaire », susceptible par exemple de lyser les bactéries.
d. Les composés précoces de la cascade du complément permettent la solubilisation des complexes immuns (un déficit héréditaire en C2 cause une « maladie des complexes immuns »).
3. Le système coagulation / fibrinolyse Le système de la coagulation aboutit au caillot (qui peut être obtenu à partir du plasma in vivo, in vitro, ou après la mort). Le résultat de la coagulation, lorsqu'elle se produit in vivo, dans une cavité vasculaire ou cardiaque, porte le nom de thrombus. Au cours de la coagulation, une cascade de protéolyses aboutit à la production de fibrine à partir du fibrinogène.
La fibrine est un composé important de l'exsudat inflammatoire ; elle limite le foyer inflammatoire et constitue une matrice sur laquelle les cellules inflammatoires peuvent se déplacer. La coagulation est en équilibre avec la fibrinolyse : la plasmine dégrade la fibrine en produisant des fragments, appelés produits de dégradation de la fibrine (ou PDF), abondants lors de la « coagulation intravasculaire disséminée » (CIVD), au cours de laquelle une coagulation se produit de façon incontrôlée dans les capillaires de l'organisme, par exemple sous l'action de toxines bactériennes.
C'est l'activation du facteur XII par des fragments tissulaires altérés qui constitue le mode de déclenchement habituel de la coagulation au cours de l'inflammation.
Choc cytokinique
[modifier | modifier le wikicode]Un choc cytokinique ("cytokine storm" en anglais) ou syndrome de libération des cytokines (SLC) est une production excessive de cytokines qui est déclenchée par un agent pathogène et qui se manifeste par une violente réponse inflammatoire du système immunitaire. Il est à l'origine des grippes malignes et de la gravité du Covid-19.
La suppuration
[modifier | modifier le wikicode]À la période cellulaire de l'inflammation aiguë, c'est l'infiltration par les polynucléaires neutrophiles qui prédomine. Lorsque qu'un infiltrat de cellules inflammatoires est identifié dans un tissu, c'est la présence de polynucléaires neutrophiles qui signe l'inflammation aiguë, et l’adjonction de l'adjectif "aiguë" par opposition à "chronique", où seuls sont retrouvées des cellules inflammatoires mononucléées (lymphocytes, macrophages/histiocytes) ou des polynucléaires éosinophiles.
Exemples :
- Appendicite aiguë
- Cholécystite aiguë
- Salpingite aiguë
La suppuration est caractérisée par la présence d'une nécrose tissulaire riche en polynucléaires neutrophiles normaux et altérés. L'accumulation de ces polynucléaires forme le pus. C'est la couleur blanche du pus qui est à l'origine de la racine leuko- du terme leucocyte (ou globule blanc). La confluence des zones de suppuration (appelée "collecte") et leur limitation forme l'abcès.
La nécrose suppurée peut entraîner une destruction de la paroi d'un organe creux et le déversement du contenu purulent de l'organe dans une cavité séreuse, par exemple :
- péritonite aiguë dans l'appendicite aiguë suppurée rompue
- péritonite aiguë dans la cholécystite aiguë suppurée rompue
- péritonite aiguë dans la salpingite aiguë suppurée rompue
- pleurite aiguë et pleurésie purulente dans l'abcès pulmonaire suppuré rompu
L’abcès
[modifier | modifier le wikicode]L'abcès se constitue en deux phases : - une phase phlegmoneuse (phlegmon) marquée par des phénomènes vasculaires et exsudatifs importants: congestion, œdème, diapédèse. Le foyer atteint est large, prolongé par une lymphangite (exemple: phlegmon des gaines des tendons fléchisseurs de la main) - une phase de collection caractérisée par la nécrose purulente ou nécrose suppurée. Les lésions sont circonscrites. Le pus occupe le centre d'une poche inflammatoire. La paroi de cette poche comprend, de dedans en dehors, les différents aspects du processus inflammatoire.
On distingue alors histologiquement : - la zone centrale, constituée par la nécrose purulente - la paroi qui comprend deux zones intriquées: la partie interne comporte des phénomènes vasculaires de congestion, d’œdème, de diapédèse; la partie externe correspond aux phénomènes de réparation (avec apparition de macrophages, néo-angiogenèse vasculaire et prolifération fibroblastique). La constitution de cette couche permet la limitation et la collection du foyer purulent.
Exemples :
- Abcès dermo-hypodermique, cutané ou sous-cutané
- Abcès péri-appendiculaire
- Abcès cérébral
L'évolution de l'abcès est favorable après détersion spontanée ou chirurgicale. Il persiste une cicatrice fibreuse. L'évolution peut être défavorable par progression de la suppuration si les phénomènes de nécrose l'emportent sur les mécanismes de collection. L'évolution peut être défavorable par fistulisation, n'aboutissant qu'à une détersion insuffisante. L'évolution peut se faire par enkystement secondaire de la nécrose, si la production de collagène est exagérée ou si la détersion n'a pas lieu. Il peut exister, dans les mêmes conditions, une calcification de la nécrose.
Comme les nécroses suppurées, les abcès peuvent entraîner une destruction de la paroi d'un organe creux et le déversement du contenu purulent de l'organe dans une cavité séreuse, par exemple :
- péritonite aiguë dans l'abcès péri-appendiculaire
- péritonite aiguë dans l'abcès sous-hépatique
- pleurite aiguë et pleurésie purulente dans l'abcès pulmonaire suppuré rompu
- méningite aiguë purulente dans l'abcès cérébral rompu
Nécrose et gangrène
[modifier | modifier le wikicode]La gangrène est une forme de nécrose. Le terme d'inflammation gangréneuse est donc impropre. La gangrène est caractérisée par une nécrose tissulaire extensive en rapport avec des obstructions vasculaires ou des infections à germes anaérobies (appendicite, cholécystite). Elle peut s'associer à des phénomènes inflammatoires massifs.
Évolution ou association avec l'inflammation chronique
[modifier | modifier le wikicode]Certaines situations pathologiques empêchent ou retardent la cicatrisation normale. C'est alors une Inflammation chronique, et l'infiltrat est à prédominance de cellules mononucléées.